

| 猜想物质的化学式 | 检验所需要的试剂 | 操作、现象和结论 | |
| ① | |||
| ② |
| 沉淀物 | Fe(OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |
| ||
| 猜想的化学物质 | 检验需要的试剂 | 操作、现象和结论 | |
| 1 | Na2SO4 | 稀盐酸和BaCl2溶液 | 取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入BaCl2溶液,如果生成白色沉淀,则原溶液是Na2SO4溶液 |
| 2 | Na2CO3 | 稀盐酸、品红试纸和澄清石灰水 | 取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体不能使湿润的品红试纸变红,但能使澄清石灰水变浑浊.原溶液是Na2CO3溶液. |
| 3 | Na2SO3 | 稀盐酸、品红试纸 | 取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体能使湿润的品红试纸变红,原溶液是Na2SO3溶液. |
| 4 | Na2SiO3 | 稀盐酸 | 取少量该溶液于试管中,滴入稀盐酸,若产生白色沉淀,则原溶液是Na2SiO3溶液. |


科目:高中化学 来源: 题型:
| A、1 mol H2的质量只有在标准状况下才约为2 g |
| B、1 mol H2和O2的混合气体,在标准状况下的体积也是约为22.4L |
| C、在20℃时,1 mol的任何气体的体积总比22.4 L大 |
| D、标准状况下SO3的体积是22.4L时,则其物质的量约是1 mol,所含分子数约是6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 可用图所示装置制取、净化、收集的气体是( )
可用图所示装置制取、净化、收集的气体是( )| A、铜和稀硝酸制一氧化氮 |
| B、用双氧水和MnO2制氧气 |
| C、石灰石和稀硫酸制CO2 |
| D、稀盐酸和MnO2制氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某有机物燃烧后产物只有CO2和H2O,可推出的结论是有机物属于烃 |
| B、某有机物燃烧后产物只有CO2和H2O,可推出的结论是有机物属于烃的含氧衍生物 |
| C、某有机物燃烧后产物只有CO2和H2O,通过测定有机物、CO2和H2O的质量,可确定有机物是否含有氧 |
| D、甲烷在同系物中含碳量最高,因而是清洁能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:
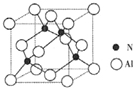 氮的化合物在无机化工领域有着重要的地位.请回答下列问题:
氮的化合物在无机化工领域有着重要的地位.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4与Ba(OH)2反应 |
| B、K2SO4与Ba(OH)2反应 |
| C、CuSO4与Ba(OH)2反应 |
| D、H2SO4与BaCO3反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com