
����Ŀ����ҵ�ϳ�����ұ��������Ʊ���ϩ������ʽΪ��![]() (g)
(g)![]()
![]() (g)+H2(g)
(g)+H2(g)
(1)��֪��
��ѧ�� | C��H | C��C | C��C | H��H |
����/kJmol��1 | 412 | 348 | 612 | 436 |
����������Ӧ�ġ�H��_____kJmol��1��
(2)�����ü������뷴Ӧ�ص㣬ѡ����������������߱���ϩƽ����ʵ�����_____��
A.���� B.���� C.��ѹ D.��ѹ E.���ʵĴ���
��ʵ�ʹ�ҵ�����г������ұ��ѽ�ȸ���Ӧ�����ұ��ѽⷴӦ����������ѧ�����ڶ���ѧ�϶����ұ���������������Թ�ҵ����Ҫʹ��Ӧ�����ⷽ�������Ҫ����_____��������߷�Ӧ��ѡ���ԡ�
�۹�ҵ�����г����ú�ѹ���������ұ������в���ˮ������CO2�İ취������ұ���ƽ��ת���ʣ����ƽ���ƶ��ĽǶȼ���˵��_____��
(3)����Ĥ��Ӧ�¼���������ʵ�ֱ߷�Ӧ�߷�������ɵ�������ͬ�¶��£�1.00mol�ұ����ݻ�Ϊ1.00L���ܱ������з�Ӧ�������Ƴ��������ұ�ƽ��ת���ʹ�ϵ��ͼ��ʾ��
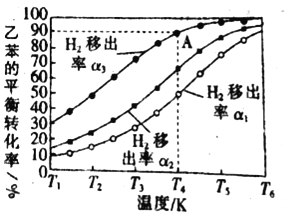
�����Ƴ�����![]()
��ͬ�¶�ʱ��1����2����3����_____��(��������������С��)ԭ����_____��
��A��ƽ�ⳣ��Ϊ0.45mol/L������Ϊ_____��
���𰸡�+124 BD ���ʵĴ��� ѹǿ���䣬���ұ������в���ˮ������CO2�������������ƽ�������ƶ�������������ұ���ƽ��ת���� ���� �����Ƴ���������������������Ũ�Ƚ��ͣ�������ƽ�������ƶ����ұ�ת�������� 94.4%
��������
��1����Ӧ�ȣ���Ӧ���ܼ��ܩ����������ܼ��ܣ����л���Ľṹ��֪��Ӧ�ǩ�CH2CH3���ܼ����멁CH��CH2��H2�ܼ���֮�
��2��������(1)����������Ϸ�Ӧ�������������ķ�Ӧ�ص�ѡ����������߱���ϩƽ����ʵ�������
��ѡ����ʵĴ���������ұ������ѡ���ԣ�
�۱���ѹǿ���䣬���ұ������в���ˮ������CO2���������Ӧ����ЧΪ����ѹǿ��ƽ���������������ķ����ƶ���
��3����ͬ�������£������Ƴ�Խ�࣬���Ƴ���Խ�ߣ�ƽ�ⷢ�������ƶ�Խ�࣬ת����Խ�ߣ�
�ڸ��ݷ�Ӧ������ʽ���ƽ�ⳣ������ƽ��ʱc(H2)�����������Ƴ��ʹ�ʽ���������Ƴ���a��
��1����Ӧ�ȣ���Ӧ���ܼ��ܩ����������ܼ��ܣ����л���Ľṹ��֪��Ӧ�ǩ�CH2CH3���ܼ����멁CH��CH2��H2�ܼ���֮����ԡ�H��(5��412+348��3��412��612��436)kJmol-1��+124kJmol-1��
��2������(1)��������֪����Ӧ�����������������ȷ�Ӧ�����»��ѹ����ʹƽ�������ƶ�����������߱���ϩƽ����ʣ�������Ӱ�챽��ϩ��ƽ����ʣ�����ѡ��BD��
�ں��ʵĴ���������ұ�����ķ�Ӧ���ʣ������ұ��ѽⷴӦ�����Թ�ҵ����Ҫʹ��Ӧ�����ⷽ����У���Ҫ���ú��ʵĴ�������߷�Ӧ��ѡ���ԣ��ʴ�Ϊ�����ʵĴ�����
�۷�Ӧ�������������ķ�Ӧ������ѹǿ���䣬���ұ������в���ˮ������CO2�������������ЧΪ����ѹǿ��ƽ���������������ķ����ƶ����ʴ�Ϊ��ѹǿ���䣬���ұ������в���ˮ������CO2�������������ƽ�������ƶ�������������ұ���ƽ��ת���ʣ�
��3����ͬ�������£������Ƴ�Խ�࣬���Ƴ���Խ�ߣ���ϵ��������Ũ��Խ�ͣ�ƽ�ⷢ�������ƶ�Խ�࣬�ұ�ת����Խ�ߣ����������Ƴ���Խ�ߣ��ұ�ת����Խ�ߣ�����1����2����3���ʴ�Ϊ�����������Ƴ���������������������Ũ�Ƚ��ͣ�������ƽ�������ƶ����ұ�ת�������ߣ�
��A��ʱ�ұ���ת����Ϊ90%��ת�������ʵ���Ϊ0.9mol����������������H2�����ʵ���Ϊ0.9mol����ƽ��ʱ��ϵ��H2�����ʵ���Ϊx��ƽ����ϵ��c(�ұ�)��0.1mol/L��c(����ϩ)��0.9mol/L��c(H2)��xmol/L��ƽ�ⳣ��![]() �����x��0.05mol�������Ƴ�����=
�����x��0.05mol�������Ƴ�����=![]() =94.4%���ʴ�Ϊ��94.4%��
=94.4%���ʴ�Ϊ��94.4%��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���������Ľᾧˮ������MCl3��6H2O������ת����ϵ�������ƶ���ȷ���ǣ� ��
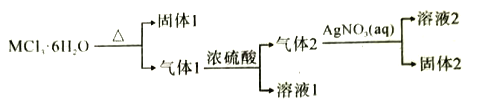
A.����1һ���Ǽ��������ᷴӦ��������ǿ�Ӧ
B.����1ͨ����ˮ����ͭ���壬�������ɫ
C.�����£���Һ2���ܽ�ͭ
D.����2��Һ�еμ�Na2S��Һ����ɫ������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��E��F��Ԫ�����ڱ���ǰ36��Ԫ�أ����ǵ�ԭ��������������A�������������Ӳ�������������������ȣ�BԪ�ػ�̬ԭ���е���ռ������������ͬ��ԭ�ӹ����ÿ�ֹ���еĵ���������ͬ��D�Ļ�̬ԭ�Ӻ���ɶԵ������dzɵ���������3����E4+���ԭ�ӵĺ�������Ų���ͬ��F�ǵ�������d��ԭ����������Ԫ�ء���ش��������⣺
��1��д��E�ļ۲�����Ų�ʽ ��
��2��A��B��C��D�縺���ɴ�С��˳��Ϊ (��Ԫ�ط���)��
��3��F(BD)4Ϊ��ɫ�ӷ��Ծ綾Һ�壬�۵�-25�� ���е�43����������ˮ���������Ҵ������ѡ������л��ܼ����������幹�ͣ��þ��������Ϊ ��F��BD֮���������Ϊ ��
��4���������ʹ���������������õ���Ҫ�о�����
����A��B��E����Ԫ�ع��ɵ�ij�����ʹ�����ϵ����۽ṹģ����ͼ1��ʾ��ͼ�����߿���Bԭ�ӵ��ӻ���������� �֣�
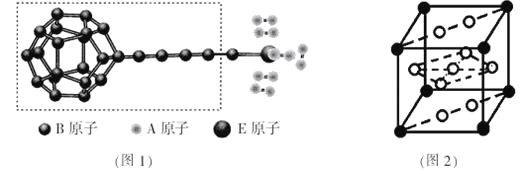
������X����ͨ������γ�����״�ṹ������ΪDZ�ڵĴ�����ϡ�Xһ������ (����)��
A��H2O B��CH4C��HF D��CO(NH2)2
��FԪ������( La)Ԫ�صĺϽ����������ϣ��þ���ľ�����ͼ2��ʾ������������һ��Fԭ�ӣ�����Fԭ�Ӷ��ھ������ϣ���þ���Ļ�ѧʽΪ_______________����֪��Ħ������ΪM g��mol-1����������Ϊa pm����NA��ʾ����٤����������þ������ܶ�Ϊ g��cm-3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ڷ��Ӿ�����ǣ�������
A. �۵���10.31����Һ̬�����磬ˮ��Һ�ܵ���
B. �۵���1070������̬�����磬����״̬�ܵ��磬������ˮ
C. �۵�3550����������ˮ��������
D. �۵���97.80������������̬�ɵ��磬�ܶ���0.97g��cm��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��K2Cr2O7��Һ�д���ƽ�⣺Cr2O72��(��ɫ)+H2O2CrO42��(��ɫ)+2H+.��֪Cr2O72����ǿ�����ԣ���CrO42����û�������ԣ�Cr3+����ɫ����K2Cr2O7��Һ�м����������ʣ�������Һ��ɫ�仯��˵������ȷ����(����)
A.��70%�����ᣬ��Һ���ɫ
B.��30%NaOH��Һ����Һ���ɫ
C.��70%��������ټ�C2H5OH����Һ�ɱ����ɫ
D.��30%NaOH��Һ����Һ���ɫ����C2H5OH�ޱ仯���ټӹ������ᣬ��Һ�������Ա仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�������ڿ��������յõ�����������A��һ�����塣ijѧϰС��Ϊ��̽����������A��������������ʵ�鷽����
������
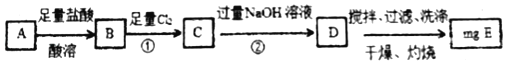
(1)���÷����Т�ͨ��Cl2��������С���Ա��Ϊ����ͨ���ڿ����г�ֽ���D������ʵ��ȷ�ⶨ������������_____(�û�ѧ����ʽ��ʾ)
(2)��������A��������7.8400g��E������Ϊ8.0000g�������ݼ��㻯����A�Ļ�ѧʽΪ_____��
������
�ٳ�ȡag������A��Ʒ��������ϡ���ᣬ�����100mL��Һ��
��ȡ20.00 mL����Һ����ƿ�У��μӼ���KSCN��Һ����Һ���ɫ���ٵμ�˫��ˮ����ɫ�պ���ȥ��ͬʱ������������(������ʾSCN-�ɱ�H2O2����������ΪN2��CO2��SO42��)
�۴�������ʧ���� b mol/LKI����Һ�ζ���ƿ�е�Fe3+���ζ��յ�ʱ����cmL KI����Һ��
(3)�÷����õ��Ķ�����������Ͳ��������ƽ����ʽ�ζ��ܡ�_____��
(4)������еμ�KSCN��Һ��Ŀ����_____��
(5)����������ʵ�鲽����õ�����ʽ�ζ��ܵ���ϴ�������رյζ������������Ͽ�ע��3��5mL��װҺ��_____���ظ�2��3�Ρ�
(6)������ܷ�ѡ�õ�����ָʾ��_____��(����������������)
(7)�е�ͬѧͨ������������϶Ը�С���ʵ����ƽ��������ۣ�����˵����������_____
A.������ʾ��HSCN�о綾���ӷ�����˸÷�������ڿ��������HSCN��������ʵ�鰲ȫ�Ե�Ҫ��
B.�����������H2O2�������������費���Դ���Ҳ�����ʵ��������κ�Ӱ�졣
C.������ʾ��Fe3+��I��֮��ķ�Ӧ�����ԵĿ��淴Ӧ����������۾ͻ���ɵζ��ⶨ��ȷ
(8)�е�ͬѧ��̼�������Ļ�ò�������Ȥ��ͨ���������Ϸ���̼��������ͨ��̼�����ƺ�������������Fe2++2HCO3��FeCO3��+H2CO3�Ƶã������÷�Ӧ��ƽ�ⳣ��K��_____(mol/L)��2�����õ��Ľɾ����£�Ksp(FeCO3)��3.20��10��11��H2CO3��Ka1��4.30��10��7��Ka2��5.61��10��11��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б��﷽ʽ��˵����ȷ���ǣ� ��
A. ��̬������̬�����Ĺ����Ƿ������
B. �Ȼ�淋ĵ���ʽ��
C. NH3��H2O��CO2��HCl �ķ����йµ��Ӷ������� CO2
D. �����ӵĺ�������Ų�ʽ 1s22s22p63s23p4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ѳ���ҵ�����еĵ�������(��Ҫ��ָNO��NO2)���Ծ������������ƻ������ǻ�����������Ҫ���⡣
(1)����������NH3��ԭ�����ɽ�NOx��ԭΪN2�����ѳ���
��֪����4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ��H=-905.9 kJ/mol
4NO(g)+6H2O(g) ��H=-905.9 kJ/mol
��N2(g)+O2(g)![]() 2NO(g) ��H=+180 kJ/mol
2NO(g) ��H=+180 kJ/mol
��H2O(g)![]() H2O(l) ��H=-44 kJ/mol
H2O(l) ��H=-44 kJ/mol
д�������£�NH3��ԭNO��Ӧ���Ȼ�ѧ����ʽ��____________��
(2)��Ư�۾���ҺΪ���ռ�������Ч�ѳ������е�NO��
��Ư�۾���Һ����Ҫ�ɷ���Ca(ClO)2�������չ����У����ĵ�Ca(ClO)2�����յ�NO�����ʵ���֮��Ϊ3��4�����ѳ���NOת��Ϊ____________��
��ijһ��ȤС���о���ͬ�¶�����ͬŨ��Ư�۾���Һ��NO�ѳ��ʵ�Ӱ�죬�����ͼ��ʾ��

ͼ�У�40��60�� NO�ѳ����������ܵ�ԭ��Ϊ____________��60��80�� NO�ѳ����½����ܵ�ԭ��Ϊ____________��
(3)��������(Na2S2O8)����ȥ��NO
��һ����NO�ڼ��Ի����б�Na2S2O8����ΪNaNO2
�ڶ����� NaNO2����������ΪNaNO3����ӦΪNO2-+S2O82-+2OH-![]() NO3-+2SO42-+H2O����ͬ�¶��£�ƽ��ʱNO2-���ѳ������������(Na2S2O8)��ʼŨ��(ָ�ڶ�����Ӧ�ij�ʼŨ��)�Ĺ�ϵ��ͼ��ʾ��
NO3-+2SO42-+H2O����ͬ�¶��£�ƽ��ʱNO2-���ѳ������������(Na2S2O8)��ʼŨ��(ָ�ڶ�����Ӧ�ij�ʼŨ��)�Ĺ�ϵ��ͼ��ʾ��
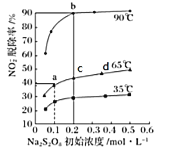
��a��b��c��d�ĵ�ƽ�ⳣ��K�ɴ�С��˳��Ϊ____________��ԭ����____________��
����a��(0.1��40%)ʱ��NO2-�ij�ʼŨ��Ϊa mol��L-1��ƽ��ʱpH=13����65��ʱ���ڶ�����Ӧ��ƽ�ⳣ��K=____________��(�ú�a�Ĵ���ʽ��ʾ)
(4)�������Ͳ��Ϲ���ѳ�NO����ͼ��ʾ��

ij�绯С�齫����A��B��Ƴ����Ե��ط�Ӧ����÷�Ӧ��������ӦΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����
A.����������Һ�еμ�������ˮ��Ag++2NH3==[Ag(NH3)2]+
B.�Ჴ���ᣨ![]() ����̼��������Һ��Ӧ��
����̼��������Һ��Ӧ��![]() +2HCO3����
+2HCO3����![]() + 2CO2��+2H2O
+ 2CO2��+2H2O
C.��ȩ��������Ӧ��CH3CHO+2[Ag(NH3)2]++2OH-![]() CH3COO��+NH4++2Ag��+3NH3+H2O
CH3COO��+NH4++2Ag��+3NH3+H2O
D.��������Һ��ͨ������CO2��2C6H5O����CO2��H2O��2C6H5OH��CO32��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com