

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:实验题
 验完成下列问题:
验完成下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Fe + Al2O3,下列说法中正确的是
2Fe + Al2O3,下列说法中正确的是| A.Fe元素的化合价升高 | B.Al被还原 |
| C.Fe2O3发生氧化反应 | D.Al是还原剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝元素在地壳中的含量高,储量丰富 |
| B.铝容易形成致密的氧化膜,抗腐蚀性能好 |
| C.铝化学性质稳定,常温下不与任何酸碱反应 |
| D.铝的冶炼技术基本成熟,可以大量生产 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

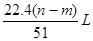
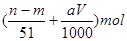
| A.2项 | B.3项 | C.4项 | D.5项 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 铍(Be)及其化合物具有相似的化学性质,如其氯化物分子内键型相同,故其氯化物晶体的熔点都较低。已知反应:BeCl2+Na2BeO2+2H2O=2NaCl+2Be(OH)2↓能完全进行,则下列推断正确的是
铍(Be)及其化合物具有相似的化学性质,如其氯化物分子内键型相同,故其氯化物晶体的熔点都较低。已知反应:BeCl2+Na2BeO2+2H2O=2NaCl+2Be(OH)2↓能完全进行,则下列推断正确的是| A.Na2BeO2溶液的pH>7,将其蒸干并灼烧后得到的残留物为BeO |
| B.BeCl2溶液的pH<7,将其蒸干并灼烧后得到的残留物可能是BeO |
| C.Be(OH)2即能溶于盐酸,又能溶于NaOH溶液 |
| D.BeCl2水溶液的导电性强,故BeCl2是离子化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.是银白色的软质金属 |
| B.能生成+3价的离子化合物 |
| C.与硝酸作用能放出氢气并生成硝酸盐 |
| D.铊的密度小于铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com