
A.检验试液中的SO42-:试液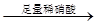 无沉淀 无沉淀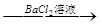 白色沉淀 白色沉淀 |
B.检验试液中的Fe2+:试液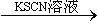 无明显现象 无明显现象 红色溶液 红色溶液 |
C.检验试液中的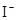 :试液 :试液 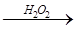 棕黄色溶液 棕黄色溶液 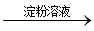 蓝色溶液 蓝色溶液 |
D.检验试液中的CO32-:试液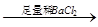 白色沉淀 白色沉淀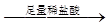 沉淀溶解 沉淀溶解 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.苯 (苯酚)—— 加入适量浓溴水,过滤 |
| B.(NO2)——通过水洗、干燥后,用向下排空气法收集 |
| C.乙烷 (乙烯)——让气体通过盛有酸性高锰酸钾溶液的洗气瓶 |
| D.乙醇 (乙酸)——加足量CaO固体,蒸馏 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.④①②③ | B.①④③② | C.①③④② | D.④②①③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.第①步中除去粗盐中的 ,依次加入的物质可以是 ,依次加入的物质可以是 溶液、 溶液、 溶液和盐酸 溶液和盐酸 |
B.第②步发生的化学反应为: |
| C.第③步工业上电解熔融的Mg(OH)2冶炼金属Mg |
| D.第④步用Na2CO3溶液吸收Br2过程中,既有溴元素被氧化也有溴元素被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 2.3 | 4.0 | 7.6 |
| 完全沉淀pH | 4.1 | 5.2 | 9.6 |
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用蒸馏的方法制取蒸馏水 |
| B.用过滤的方法除去NaCl溶液中含有的少量Na2SO4 |
| C.用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D.用加热、蒸发的方法可以除去NaCl中的CaCl2、MgCl2等杂质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.BaCl2溶液、Ba(NO3)2溶液、Na2CO3溶液 |
| B.NaCl溶液、Ba(NO3)2溶液、Na2CO3溶液 |
| C.KCl溶液、 Ba(NO3)2溶液、MgCl2溶液 |
| D.NaCl溶液、K2CO3溶液、Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物安全沉淀 | 3.2 | 9.0 | 6.7 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


| | 乙酸 | 1-丁醇 | 乙酸丁酯 |
| 熔点(℃) | 16.6 | -89.5 | -73.5 |
| 沸点(℃) | 117.9 | 117 | 126.3 |
| 密度(g/cm3) | 1.05 | 0.81 | 0.88 |
| 水溶性 | 互溶 | 可溶 (9g/100g水) | 微溶 |




查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com