
【题目】从海水中提取镁的工业生产流程如下:
![]()
下列说法错误的是
A.此法的优点之一是原料来源丰富
B.该提取镁的过程中涉及置换、分解、复分解和氧化还原反应
C.步骤①②③的目的是从海水中提取无水MgCl2
D.步骤②中加盐酸的离子方程式为Mg(OH)2+2H+=Mg2++2H2O
科目:高中化学 来源: 题型:
【题目】在催化剂作用下,用乙醇制乙烯,乙醇转化率和乙烯选择性(生成乙烯的物质的量与乙醇转化的物质的量的比值)随温度、乙烯进料量(单位: ![]() )的关系如图所示(保持其他条件相同)。
)的关系如图所示(保持其他条件相同)。
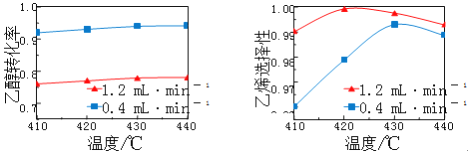
在410~440℃温度范围内,下列说法不正确的是
A. 当乙醇进料量一定,随乙醇转化率增大,乙烯选择性升高
B. 当乙醇进料量一定,随温度的升高,乙烯选择性不一定增大
C. 当温度一定,随乙醇进料量增大,乙醇转化率减小
D. 当温度一定,随乙醇进料量增大,乙烯选择性增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号中注明的方法分离下列各组混合物,其中不正确的是( )
A. 汽油和煤油(蒸馏) B. 食盐中的沙子(溶解过滤)
C. 氯化钠和水(过滤) D. 花生油和水(分液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙二醇是重要的化工原料,利用甘油制备二元醇符合绿色化学要求.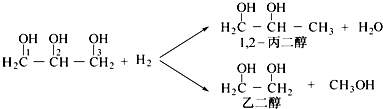
利用1,2﹣丙二醇可制得乳酸〔CH3CH(OH)COOH〕,乳酸与上述反应中的某一产物B可以反应,转换关系如下.已知A的碳原子数与乳酸相同,E、F为链状高分子化合物.请回答下列问题: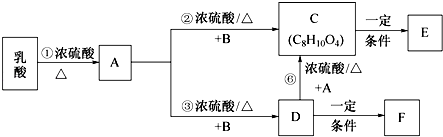
(1)反应①的反应类型是反应,A中所含官能团名称是 .
(2)B在一定条件下反应生成分子式为C2H4O的有机物,该物质不能发生银镜反应,核磁共振氢谱中只有一个峰,写出该物质的结构简式 .
(3)F具有良好的光学性能和亲水性可作为隐形眼镜的材料,写出由D制备F的化学方程式 .
(4)写出1,2﹣丙二醇制备乳酸的合成路线 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用硫酸厂烧渣(含铁的氧化物和少量FeS及SiO2)制碱式硫酸铁的流程如下:

(1)SO2与过量NaOH溶液反应的离子方程式为_____________。
(2)滤渣的主要成分为_________(填化学式)。
(3)反应1中加双氧水的目的是将Fe2+氧化为Fe3+,该反应的离子方程式为________。
(4)碱式硫酸铁的化学式为Fex(OH)y(SO4)z·nH2O,为确定其组成进行如下实验:
①称取1.6920g样品溶于足量的稀盐酸中;
②加足量的BaCl2溶液,过滤、洗涤、干燥、称重,得固体质量为2.3300g;
③向步骤②的滤液中加过量的NaOH溶液,过滤、洗涤、灼烧、称重,得固体质量为0.6400g。
根据以上实验数据确定该碱式硫酸铁的化学式_________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用质量分数为98%、密度为1.84g/mL的浓硫酸来配制480mL0.2mol/L 的稀硫酸。可供选择的仪器有: ①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙。完成下列问题:
(1)上述仪器中,在配制稀硫酸时不需要用到的是______ (填仪器序号)。
(2)配制过程中需选用的容量瓶规格为_____mL,经过计算,需要量取的浓硫酸体积为_____mL。
(3)在配制过程中,下列操作使所配溶液浓度偏高的是______ (填字母)。
a.未洗涤稀释浓硫酸所用的烧杯和玻璃棒
b.为防止变质,稀释后的硫酸溶液立即就转移到容量瓶中
C.移液前,容量瓶中含有少量蒸馏水
d.定容时,俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定量混合气体发生下列反应:aA(g)+bB(g)cC(g)+dD(g),达到平衡后,测得C气体的浓度为0.5mol/L.当在恒温下,将密闭容器的体积缩小为 ![]() ,再达平衡时,测得C气体的浓度为0.9mol/L.则下列叙述正确的是( )
,再达平衡时,测得C气体的浓度为0.9mol/L.则下列叙述正确的是( )
A.反应速率降低
B.平衡向右移动
C.B的转化率提高
D.a+b<c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为了检验浓硫酸与木炭粉在加热条件下反应:![]() ,产生的所有气体产物,选用了下图所示实验装置。
,产生的所有气体产物,选用了下图所示实验装置。
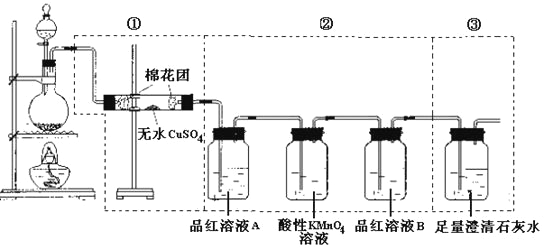
(1)①中无水硫酸铜的作用是___________。
(2)②中酸性KMnO4溶液的作用是______________________。
(3)②中两次用到品红溶液,它们的作用分别是A________、B________。
(4)③中发生反应的离子方程式是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com