
【题目】下列说法不正确的是
A.![]() 属于有机物,因此是非电解质
属于有机物,因此是非电解质
B.石油裂化和裂解的目的均是为了将长链烃转化为短链烃
C.煤的气化,液化和干馏都是化学变化
D.等质量的乙烯,丙烯分别充分燃烧,所耗氧气的物质的量一样多
科目:高中化学 来源: 题型:
【题目】镁及其合金广泛应用于国防生产中。
(1)工业上是通过电解熔融状态![]() 的方法冶炼金属镁的,则
的方法冶炼金属镁的,则![]() 的电子式为___;工业上不用电解熔融MgO来冶炼镁的原因是_____。
的电子式为___;工业上不用电解熔融MgO来冶炼镁的原因是_____。
(2)氢化镁是一种危险化学品。遇湿易燃,其原因是____。
(3)高纯度氧化镁在医药,建筑行业有着广泛的应用,硫酸镁还原热解制备高纯氧化镁是一种新生产工艺,以菱镁矿(主要成分为![]() ,含少量
,含少量![]() )为原料,制备高纯氧化镁的流程如图(已知
)为原料,制备高纯氧化镁的流程如图(已知![]() 、
、![]() ):
):
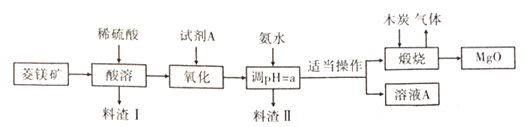
①酸浸前对矿石进行粉碎的好处是____。试剂A是一种绿色氧化剂。常温下为液态,写出“氧化”过程中发生反应的离子方程式_____。
②为除尽杂质,a的取值应不小于___(当杂质离子浓度小于![]() 时,可认为已除尽;
时,可认为已除尽;![]() ≈0.2)。
≈0.2)。
③煅烧过程中可发生多个反应。试写出氧化剂与还原剂按物质的量为2:1的比例恰好反应时的化学方程式_____,反应生成的气体均为____(填“酸性”或“碱性”)氧化物。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)CH≡CCH(CH3)2系统命名法命名为 。
(2) 2,3-二甲基-1-丁烯的结构简式为 。
(3)支链只有一个乙基且式量最小的烷烃的结构简式为 。
(4)某烃分子式为C6H14,若该烃不可能由炔烃与氢气加成得到则该烃的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中含有的可溶性杂质硫酸盐、氯化钙和氯化镁,某同学利用给定试剂NaOH溶液、BaCl2溶液、Na2CO3溶液和盐酸,设计了如下实验流程:
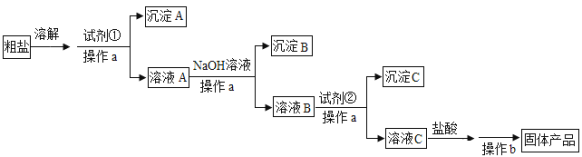
请回答:
(1)操作a和操作b的名称依次是______。
(2)试剂①是______。
(3)加入NaOH后,发生反应的离子方程式是___________。
(4)加入试剂②后,发生反应的离子方程式是___________。
(5)加入盐酸的作用是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示。下列说法正确的是( )
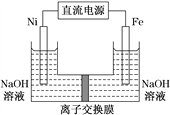
A. 铁是阳极,电极反应为Fe-2e-+2OH-===Fe(OH)2
B. 电解一段时间后,镍电极附近溶液的c(OH-)减小
C. 若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO![]()
D. 每制得1 mol Na2FeO4,理论上可以产生67.2 L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示代表周期表中的几种短周期元素,下列说法中错误的是()
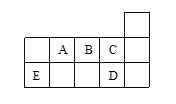
A. ED4分子中各原子均满足8电子稳定结构
B. AD3和ED4两分子的中心原子均为sp3杂化
C. C、D气态氢化物稳定性强弱为C>D
D. A、B、C电负性大小顺序为C>A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为元素周期表中原子序数依次增大的前36号元素,基态A原子的价电子排布式为nsnnpn,C原子基态时2p能级上有2个未成对的电子,D元素的原子结构中3d能级上成对电子数是未成对电子数的3倍,B与E同主族。
请回答下列问题:
(1)基态A原子的价电子轨道表示式为_______,其电子占据的最高能级的电子云形状为________。
(2)B、C、E三种元素的电负性由大到小的顺序为________(用元素符号表示)
(3)E的含氧酸有两种形式,化学式分别为H3EO3和H3EO4,则二者酸性强弱H3EO3_____H3EO4(填“>”“<”或“=”)
(4)D单质在AC气流中轻微加热,生成无色挥发性液态D(AC)4配合物,该配合物的晶体类型是_________。
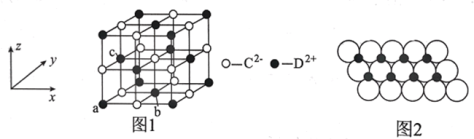
(5)DC晶胞结构如图1所示,离子坐标参数a为(0,0,0),b为(![]() ,
,![]() ,0),则c离子的坐标参数为________;一定温度下,DC晶体可自发地分散并形成“单层分子”,可以认为C2–作密置单层排列,D2+填充其中,如图2所示,C2–离子的半径为xm,阿伏加德罗常数的值为NA,则每平方米面积上分散的该晶体的质量为_____g(用含x、NA的代数式表示)。
,0),则c离子的坐标参数为________;一定温度下,DC晶体可自发地分散并形成“单层分子”,可以认为C2–作密置单层排列,D2+填充其中,如图2所示,C2–离子的半径为xm,阿伏加德罗常数的值为NA,则每平方米面积上分散的该晶体的质量为_____g(用含x、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化合物(a)![]() 、(b)
、(b)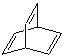 、(c)
、(c)![]() ,(d)
,(d)![]() ,下列说法不正确的是 ( )
,下列说法不正确的是 ( )
A. a、b、c、d互为同分异构体B. 除a外均可发生加成反应
C. c中所有原子不可能处于同一平面D. 一氯代物同分异构体最多的是c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以海水晒盐后所得苦卤(溶质主要含MgCl2,还有NaCl等)为原料制取金属镁的流程如图:
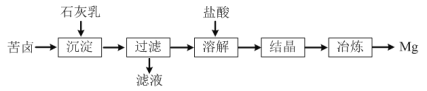
(1)“沉淀”反应的化学方程式为___。
(2)“溶解”反应的离子方程式为___。
(3)工业上冶炼镁时采用的方法是___(填字母)。
a.电解熔融MgCl2
b.用氢气还原MgCl2
c.加热分解MgCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com