
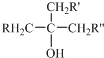 中的-OH不能被氧化.
中的-OH不能被氧化.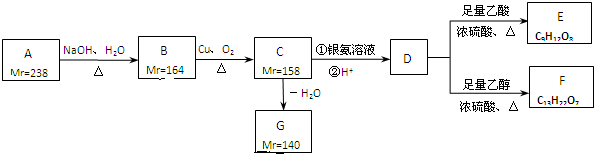
| 164-158 |
| 2 |
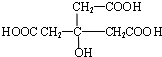 ,逆推可得C的结构简式为
,逆推可得C的结构简式为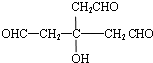 、B为
、B为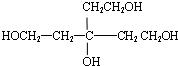 ,D发生消去反应生成G为
,D发生消去反应生成G为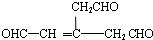 ,D的相对分子质量与E相差42,则1分子与1分子乙酸发生酯化反应生成E,由F的分子式可知1分子D与3分子乙醇发生酯化反应生成F,故E为
,D的相对分子质量与E相差42,则1分子与1分子乙酸发生酯化反应生成E,由F的分子式可知1分子D与3分子乙醇发生酯化反应生成F,故E为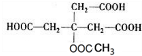 ,F为
,F为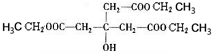 .A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为
.A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为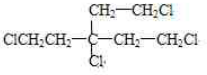 ,据此解答.
,据此解答.| 164-158 |
| 2 |
 ,逆推可得C的结构简式为
,逆推可得C的结构简式为 、B为
、B为 ,D发生消去反应生成G为
,D发生消去反应生成G为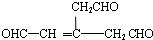 .D的相对分子质量与E相差42,则1分子与1分子乙酸发生酯化反应生成E,由F的分子式可知1分子D与3分子乙醇发生酯化反应生成F,故E为
.D的相对分子质量与E相差42,则1分子与1分子乙酸发生酯化反应生成E,由F的分子式可知1分子D与3分子乙醇发生酯化反应生成F,故E为 ,F为
,F为 .A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为
.A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为 .D的相对分子质量与E相差42,则1分子与1分子乙酸发生酯化反应生成E,由F的分子式可知1分子D与3分子乙醇发生酯化反应生成F,
.D的相对分子质量与E相差42,则1分子与1分子乙酸发生酯化反应生成E,由F的分子式可知1分子D与3分子乙醇发生酯化反应生成F, ,含有的官能团是:氯原子,故答案为:氯原子;
,含有的官能团是:氯原子,故答案为:氯原子; ,C为
,C为 ,B中所有官能团中其中1个羟基没有发生反应,故b错误;
,B中所有官能团中其中1个羟基没有发生反应,故b错误; )发生消去反应生成G,生成G只有1种产物,故c正确;
)发生消去反应生成G,生成G只有1种产物,故c正确;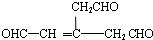 ,其中1个不饱和碳原子上连接2个-CH2CHO,不存在顺反异构现象,故d错误,
,其中1个不饱和碳原子上连接2个-CH2CHO,不存在顺反异构现象,故d错误,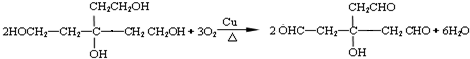 ,
, ;
;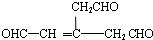 )互为同分异构体,1mol H与足量氢氧化钠溶液反应消耗2mol NaOH,含有2个酚羟基,另外侧链可为-CH2OH,当2个-OH处于邻位,-CH2OH有2种位置,当2个-OH处于均为,-CH2OH有3种位置,当2个-OH处于对位,-CH2OH有1种位置,含有6种,另外侧链可为-OCH3,也含有6种,故共含有12种;
)互为同分异构体,1mol H与足量氢氧化钠溶液反应消耗2mol NaOH,含有2个酚羟基,另外侧链可为-CH2OH,当2个-OH处于邻位,-CH2OH有2种位置,当2个-OH处于均为,-CH2OH有3种位置,当2个-OH处于对位,-CH2OH有1种位置,含有6种,另外侧链可为-OCH3,也含有6种,故共含有12种;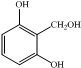 等,
等, 等;
等; ,
, .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、标准状况下,1mol水的体积是22.4L |
| B、1mol任何气体,体积均为22.4L |
| C、0.3 molN2、0.7 molO2 在标准状况下的总体积约为22.4L |
| D、1molN2在25℃和101KPa时,体积约为22.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向NH4Fe(SO4)2溶液中加入过量Ba(OH)2溶液:2NH4++Fe3++2SO42-+2Ba2++5OH-=2BaSO4↓+Fe(OH)3↓+2NH3?H2O |
| B、向NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| C、向Na2CO3溶液中加入FeCl3溶液:Fe3++3CO32-+3H2O=Fe(OH)3↓+3HCO3- |
| D、Na2SO3溶液在空气中变质:2SO32-+O2=2SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
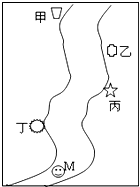 如图所示,在一条鱼、虾几乎绝迹的小河边,从上游到下游依次有甲、乙、丙、丁四座工厂,各厂排放的废水里都只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水监测时发现:①甲处河水呈乳白色;②乙处河水呈红褐色;③丙处河水由浑变清;④丁处产生气泡,河水仍澄清. 四座工厂排出的废水里含有的污染物分别为:
如图所示,在一条鱼、虾几乎绝迹的小河边,从上游到下游依次有甲、乙、丙、丁四座工厂,各厂排放的废水里都只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水监测时发现:①甲处河水呈乳白色;②乙处河水呈红褐色;③丙处河水由浑变清;④丁处产生气泡,河水仍澄清. 四座工厂排出的废水里含有的污染物分别为:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
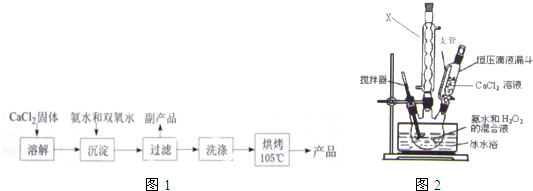
| 实验序号 | 第1次 | 第2次 | 第3次 | 第4次 |
| 消耗KMnO4体积/mL | 19.98 | 20.02 | 20.20 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com