

 O2(g)=CO(g)�Ħ�H���������ʵ�顢���ø�˹���ɼ�����÷�Ӧ�Ħ�H������ʱ��Ҫ��õ�ʵ��������________��
O2(g)=CO(g)�Ħ�H���������ʵ�顢���ø�˹���ɼ�����÷�Ӧ�Ħ�H������ʱ��Ҫ��õ�ʵ��������________�� O2(g)=CO(g)�Ħ�H����Ҫ��õ�ʵ��������̼��CO��ȼ���ȡ�
O2(g)=CO(g)�Ħ�H����Ҫ��õ�ʵ��������̼��CO��ȼ���ȡ�


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��sp2�ӻ�����γɦҼ���δ�ӻ���2p����γɦм� |
| B��sp2�ӻ�����γɦм���δ�ӻ���2p����γɦҼ� |
| C��C��H֮����sp2�γɵĦҼ���C��C֮����δ�μ��ӻ���2p����γɵĦм� |
| D��C��C֮����sp2�γɵĦҼ���C��H֮����δ�μ��ӻ���2p����γɵĦм� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��8�����ӵ�̼ԭ�ӵĺ��ط��ţ�12C |
B��HF�ĵ���ʽ��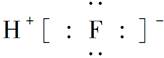 |
C��Cl�����ӵĽṹʾ��ͼ��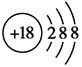 |
| D��CO2�Ľṹʽ��O=C=O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���Ҽ��ܵ����γɣ����м�һ�����ܵ����γ� |
| B���Ҽ������Ƽ�����ת���м�һ�������Ƽ�����ת |
| C��˫����һ����һ���Ҽ���һ���м���������һ����һ���Ҽ��������м� |
| D�����嵥����һ�����ڦҼ������ܴ��ڦм� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2O2��NaOH | B��CH3COONa��NaOH |
| C��CCl4��H2O | D��CO2��H2O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ɷ�����ɵ�������һ�����ڹ��ۼ� |
| B���ɷǽ���Ԫ����ɵĻ�����һ���ǹ��ۻ����� |
| C���Ǽ��Լ�ֻ�ܴ�����˫ԭ�ӵ��ʷ����� |
| D�����ַǽ���Ԫ��ԭ�Ӽ䲻�����γ����Ӽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 SO2(g)����H����297.16 kJ��mol��1��
SO2(g)����H����297.16 kJ��mol��1�� 2SO3(g)����H����196.6 kJ��mol��1��
2SO3(g)����H����196.6 kJ��mol��1��| A��1 mol SO2(g)�������ܺʹ���1 mol S(s)��1 mol O2(g)�������ܺ� |
| B����2 mol SO2(g)��1 mol O2(g)��һ�������³�ַ�Ӧ���ų�196.6 kJ������ |
| C��S(g)��O2(g)=SO2(g)����H����Q��QֵС��297.16 kJ |
| D����1 mol S(s)��ȫת��ΪSO3(g)ʱ(������������ʧ)���ų�395.46 kJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2HCl(g)=H2(g)��Cl2(g)�ķ�Ӧ�Ȧ�H<0 |
| B��H(g)��Cl(g)=HCl(g)����H����431 kJ��mol��1 |
| C����ͬ�����£�H2(g)��Cl2(g)=2HCl(g)�ڹ��պ͵�ȼ�����µĦ�H��� |
| D��H2(g)��Cl2(g)=2HCl(g)����H����183 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
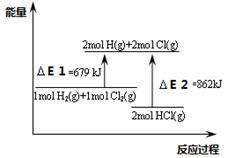
| A����E2��2mol HCl(g)���ܼ��� |
| B���÷�Ӧ���Ȼ�ѧ����ʽΪ��H2(g)+Cl2(g)��2HCl(g)��H ����183KJ.mol-1 |
| C��ͨ�������H2��Cl2��Ͳ��ᷴӦ |
| D���÷�Ӧ��һ�����ȷ�Ӧ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com