
【题目】下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
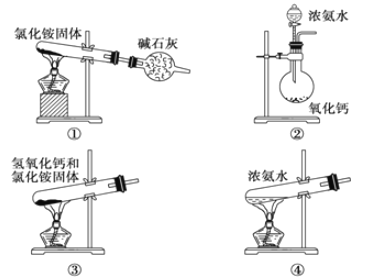
A. ①②B. ②③C. ③④D. ①③
【答案】D
【解析】
①氯化铵不稳定受热易分解,但是氨气与氯化氢遇冷又极易反应生成氯化铵固体;
②CaO遇水生成Ca(OH)2,同时放出大量热量,有利于氨气的生成;
③固体加热制气体时,试管口应略向下倾斜;
④浓氨水易挥发,加热能够促进氨气的逸出。
①氯化铵不稳定受热易分解,但是分解产生的氨气与氯化氢遇冷又极易反应生成氯化铵固体,因此不能用于制备氨气,①错误;
②向CaO中滴加浓氨水,CaO遇水生成Ca(OH)2,同时放出大量热量,有利于浓氨水中的氨气逸出,②正确;
③固体加热制气体时,试管口应略向下倾斜,使产生的水能够流出,以免水蒸气遇冷产生的液体水回流,使试管炸裂,损坏试管,因此利用氯化铵和氢氧化钙固体加热制取氨气需试管口应略向下倾斜,③错误;
④浓氨水易挥发,加热能够促进氨气的逸出,可以用来制备氨气,④正确;
可见上述实验装置图中错误的是①③,故合理选项是D。


科目:高中化学 来源: 题型:
【题目】阿司匹林(化合物L)是人们熟知的解热镇痛药物。一种长效、缓释阿司匹林(化合物P)的合成路线如图所示:

已知:①HC![]() CH+RCOOH
CH+RCOOH![]() RCOOCH=CH2
RCOOCH=CH2
②RCOOR’+R”OH![]() RCOOR”+R’OH
RCOOR”+R’OH
(1)B中的官能团是__。
(2)C的结构简式是__。
(3)D→E的反应类型是__。
(4)E→G的化学方程式是__。
(5)已知:H是芳香族化合物。在一定条件下2B→K+H2O,K的核磁共振氢谱只有一组峰。J→L的化学方程式是__。
(6)L在体内可较快转化为具有药效的J,而P与L相比,在体内能缓慢持续释放J。
①血液中J浓度过高能使人中毒,可静脉滴注NaHCO3溶液解毒。请用化学方程式解释NaHCO3的作用:__。
②下列说法正确的__(填字母)。
a.P中的酯基在体内可缓慢水解,逐渐释放出J
b.P在体内的水解产物中没有高分子化合物
c.将小分子药物引入到高分子中可以实现药物的缓释功能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是s能级和p能级的电子云轮廓图,试回答问题。


(1)s电子云轮廓图呈________形,每个s能级有________个原子轨道;p电子云轮廓图呈________状,每个p能级有________个原子轨道,其能量关系为____________(填“相同”或“不相同”)。
(2)元素X的原子最外层的电子排布式为nsnpn+1,原子中能量最高的是________电子;元素X的名称是____,它的氢化物的电子式是________。
(3)若元素Y的原子最外层的电子排布式为nsn-1npn+1,那么Y的元素符号应为________,原子的电子排布图为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:
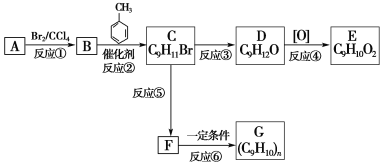
已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法正确的是( )
A.4.6gNa完全转化成Na2O和Na2O2的混合物,生成物中阴离子总数为0.1NA
B.标准状况下,22.4L丙烷所含共用电子对数为8NA
C.标准状况下,2.24LCl2溶于水,转移的电子数目为0.1NA
D.常温下,1L0.1mol·L-1NH4NO3溶液中含有的NH4+数是0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把图2中的物质补充到图1中,可得到一个完整的氧化还原型离子方程式(未配平)。
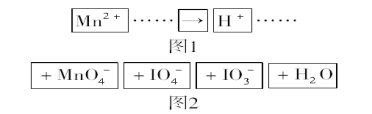
对该氧化还原反应型离子方程式,说法不正确的是( )
A.IO4-作氧化剂具有氧化性
B.氧化剂和还原剂的物质的量之比为5∶2
C.若有2molMn2+参加反应时则转移10mol电子
D.氧化性:MnO4->IO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物其结构简式为![]() ,关于该有机物下列叙述正确的是
,关于该有机物下列叙述正确的是
A. 不能使酸性KMnO4溶液褪色
B. 不能使溴水褪色
C. 在加热和催化剂作用下,最多能和4 mol H2反应
D. 易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了如下实验流程:在一个小烧杯里,加入20gBa(OH)2·8H2O晶体和10gNH4Cl晶体,然后将小烧杯放在事先已滴有3~4滴水的玻璃片上,并立即用玻璃棒迅速搅拌。实验流程示意图如图所示,回答下列问题:

(1)实验中玻璃棒的作用是___________________。
(2)浸有稀硫酸的棉花的作用是___________________。
(3)请写出该反应的化学反应方程式:______________________________。
(4)通过______________________________现象,说明该反应为___________________(填“吸热”或“放热”)反应,这是因为反应物的总能量___________________(填“>”“<”或“=”)生成物的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置。它可直接将化学能转化为电能,甲烷燃料电池以KOH溶液为电解质,其总反应的化学方程式为:CH4+2O2+2OH-===CO32—+3H2O。
(1)负极上的电极反应为____________________________________。
(2)消耗标准状况下的5.6 L O2时,有________ mol电子发生转移。
(3)开始放电时,正极附近溶液的pH________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com