
【题目】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是____________。
(2)该反应中,发生还原反应的过程是______________→____________。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目_____________。
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下的体积为 。
(5)已知I-、Fe2+、SO2、Cl-、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为:SO2>I->H2O2>Fe2+>Cl-,则下列反应不能发生的是( )
A.2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
B.I2+SO2+2H2O=H2SO4+2HI |
C.H2O2+H2SO4=SO2↑+O2↑+2H2O |
D.2Fe3++2I-=2Fe2++I2 |
【答案】(1)H2O2(2)H2CrO4→Cr(OH)3
(3)
(4)3.36L(5)C
【解析】试题分析:(1)由H2O2→O2,氧元素化合价从-1→0价,化合价升高,H2O2作还原剂。
(2)所给物质中H2CrO4中铬元素的化合价降低发生还原反应作氧化剂,H2CrO4→Cr(OH)3。
(3)由上述分析可知,在该反应中H2O2→O2,氧元素化合价从-1→0价,H2CrO4中铬元素的化合价降低发生还原反应作氧化剂,H2CrO4→Cr(OH)3。依据化合价升降总数相等配平方程式可得: 。
。
(4)由上述反应可知每转移6 mol电子可生成3×22.4 L的O2,故转移0.3 mol电子时,所得气体的体积为:0.3mol÷6mol×3×22.4 L="3.36" L。故答案为:3.36L;
(5)根据氧化还原反应的规律:氧化性:氧化剂>氧化产物;还原性:还原剂大于还原产物。强氧化剂与强还原剂发生反应产生具有弱氧化性和弱还原性的物质。A.若反应2Fe3++SO2+2H2O=2Fe2+ + SO42- +4H+可以发生,则还原性:SO2>Fe2+,与题意吻合,故A正确;B.若反应I2+SO2+2H2O=H2SO4+2HI可以发生,则还原性:SO2>I-,与题意吻合,故B正确;C.若反应H2O2+H2SO4=SO2+O2↑+H2O可以发生,则还原性:H2O2>SO2,与题意不吻合,故C错误;D.若反应2Fe3++2I-=2Fe2++I2可以发生,则还原性:I-大于Fe2+,与题意吻合,故D正确。故选C。


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
【题目】15.8g KMnO4氧化密度为1.19 g/cm3,溶质质量分数为36.5%的HCl,反应方程式如下:2KMnO4 + 16HCl =2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O。
(1)该盐酸中HCl的物质的量浓度是______________________________。
(2)被氧化的HCl的物质的量为________________________。
(3)求产生的Cl 2在标准状况下的体积(依据化学方程式进行计算,要求写出计算过程)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,挪威和荷兰正在开发一种新能源﹣﹣盐能.当海水和淡水混合时,温度将升高0.1℃,世界所有入海口的这种能源相当于电力需求的20%,海水和淡水混合时,温度升高最可能的原因是( )
A.由于浓度差产生放热
B.发生了水分解反应
C.发生了盐分解反应
D.盐的溶解程度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质间的反应与反应类型不相符的是( )
A. 乙烯与溴水(加成反应)B. 苯与浓硝酸(取代反应)
C. 乙醇与乙酸((酯化反应)D. 乙醇与氧气(取代反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究氮、磷等单质及其化合物的反应有重要意义.
(1)试判断用于汽车净化的一个反应2NO(g)+2CO(g)═N2(g)+2CO2(g),在298K、100kPa下能否自发进行(填“能”或“否”).已知:在298K、100kPa下该反应的△H=﹣113.0kJmol﹣1 , △S=﹣145.3Jmol﹣1K﹣1 .
(2)25℃下,将a molL﹣1的氨水与0.005molL﹣1的硫酸等体积混合,反应平衡时溶液中c(NH4+)=2c(SO42﹣),用含a的代数式表示NH3H2O的电离常数Kb= .
(3)25℃时,Ksp(BaSO4)=1.1×10﹣10 , Ksp(BaCO3)=2.6×10﹣9 , 现将BaCl2溶液滴入浓度均为0.01molL﹣1的Na2SO4和Na2CO3的混合溶液中,当两种沉淀共存时,溶液中c (CO32﹣):c(SO42﹣)=(不考虑CO32﹣的水解)
(4)次磷酸(H3PO2)是一种一元中强酸,重要的精细化工产品.
①写出次磷酸的电离方程式: .
②已知某温度下0.01mol/L的NaOH溶液pH=10,将该NaOH溶液与等浓度等体积的H3PO2溶液混合,混合后溶液pH=7,则此时c(OH﹣)﹣c(H3PO2)= . 该温度下将pH=a的盐酸Vaml与pH=b的氢氧化钠Vbml混合后溶液呈中性,且a+b=10,则Va:Vb= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在标准状况下,某气体的体积为33.6L,气体的物质的量是 , 若是CO2气体,则该气体的质量是 , 若是CO和CO2气体总中质量为58克,其中氧原子个数是NA , 混合气体中碳氧原子个数比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国家质检部门检出人们端午节包粽子的“返青粽叶”多以胆矾(化学式为CuSO4·5H2O)为添加剂,长期食用有害健康,请问胆矾是一种( )
A. 氧化物B. 盐C. 碱D. 酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是( )
A. 银、二氧化硫、硫酸、纯碱、食盐
B. 碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C. 氢气、干冰、硝酸、烧碱、硝酸钾
D. 铜、氧化铜、醋酸、石灰水、碳酸氢钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法,不正确的是
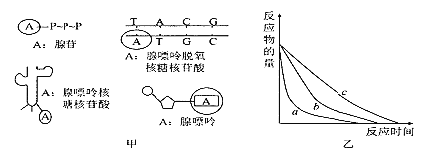
A. 甲图四种化合物中“0”内A所对应含义的解释有一个是错误的
B. 硝化细菌体内含有甲图中的四种化合物
C. 若乙图表示某种酶在不同温度下催化某反应的效果图,则温度a>b>c
D. 若乙图表示不同浓度的某种酶催化某反应的效果图,则酶浓度a>b>c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com