
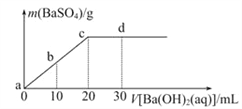
【题目】常温下,向0.1mol/L的H2SO4溶液中逐滴加入0.1mol/L的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示,下列说法中正确的是
A. a~d溶液的pH:a<b<c<d
B. a~d溶液的导电能力:a<b<c<d
C. b处溶液的c(H+)与d处溶液的c (OH-)相等
D. c处溶液和d处溶液均呈碱性
【答案】A
【解析】试题分析:A、硫酸和氢氧化钡的反应方程式为H2SO4+Ba(OH)2=BaSO4↓+2H2O,随着氢氧化钡溶液的加入,溶液中氢离子的浓度逐渐降低,溶液的PH 值逐渐增大,当达到c点时,硫酸和氢氧化钡恰好反应生成硫酸钡和水,溶液的PH=7,继续滴加氢氧化钡溶液,溶液的PH>7,A正确.
B、导电能力与溶液中自由移动离子的浓度有关,离子浓度越大,导电能力越强,随着氢氧化钡溶液的加入,溶液中硫酸根离子和氢离子逐渐减少,当达到c点时,硫酸和氢氧化钡恰好反应生成硫酸钡和水,溶液的导电性最小,继续滴加氢氧化钡溶液时,氢氧化钡是可溶性的强电解质,溶液中自由移动的离子浓度增大,导电性逐渐增强,所以导电能力是先减小后增大,B错误.
C、硫酸和氢氧化钡的反应方程式为H2SO4+Ba(OH)2=BaSO4↓+2H2O,溶液混合前硫酸的物质的量浓度和氢氧化钡的物质的量浓度相同,根据图象知,滴加氢氧化钡溶液20mL时,两种溶液恰好反应,所以硫酸的体积为20mL,b点时,氢离子的物质的量浓度=![]() =
=![]() mol/L;d点时氢氧根离子的物质的量浓度=
mol/L;d点时氢氧根离子的物质的量浓度=![]() =
=![]() mol/L,所以两处的物质的量浓度不同,C错误.
mol/L,所以两处的物质的量浓度不同,C错误.
D、c处,硫酸和氢氧化钡恰好反应生成硫酸钡和水,溶液呈中性;d处氢氧化钡溶液过量导致溶液呈碱性,D错误,选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列实验中能得到Fe2O3 的是( )
A.铁丝在纯氧中燃烧B.红热的铁和水蒸气反应
C.将Fe2(SO4)3 溶液蒸干后灼烧D.加热氢氧化铁固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面关于生物体内化合物的描述,错误的是
A. 磷脂是所有细胞必不可少的脂质
B. 组成酶的基本单位之间都是通过肽键连接的
C. 淀粉、糖原分子结构不同主要是由于它们的空间结构不同
D. 参与构成ATP分子和RNA分子的五碳糖相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列关于H2S和SO2的说法正确的是______________
A.两气体都可用浓硫酸干燥
B.两气体均可以用NaOH溶液吸收
C.两气体按体积比1:2 混合可完全转化为S
D.将两气体通入溴水或酸性KMnO4溶液中,可通过颜色变化鉴别两气体
(2)目前治理汽车尾气是在催化剂条件下发生反应2NO+2CO![]() N2+2CO2,现在实验室模拟上述反应,己知在t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:
N2+2CO2,现在实验室模拟上述反应,己知在t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:
①这段时间内CO的反应速率为_________________ 。
②该反应平衡常数______________(保留两位有效数字)。
③平衡后再向密闭容器通入0.4molCO和0.4molCO2,平衡将_____________(填“正向”、“逆向”或“不”)移动。判断理由是_________________。
④若升温发现体系气体平均相对分子质量增大,则该反应的△H______0(填“>”、“<”或“=”)。
⑤维持条件不变,向平衡后的容器再充入0.2molNO和0.1molCO,达到新平衡,则与原平衡相比NO的转化率____________ (填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液一定是碱性的是 ( )
A. 溶液中c(OH-)>c(H+) B. c(OH-)>1×10-7mol/L
C. 溶液中含有OH- D. pH=8的某电解质的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列转化不能通过一步反应实现的是( )
A.H2S+O2→SO2
B.SO2+H2O→H2SO3
C.S+O2→SO3
D.SO3+H2O→H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com