
����Ŀ���״���CH3OH������Ҫ���ܼ������ȼ����CO��H2�Ļ�������׳ƺϳ�����������һ���������Ʊ�CH3OH��
��1�������ܱ������г���CO��H2���о�������������ʱ�¶ȶԺϳɼ״���ӦӰ�죺CO(g)+2H2(g) ![]() CH3OH(g)��ʵ������ͼ��ʾ��
CH3OH(g)��ʵ������ͼ��ʾ��

���¶ȸߵͱȽϣ�T1____T2��
�������ж���ȷ����______________��
A.�÷�Ӧ�Ƿ��ȷ�Ӧ
B.�÷�Ӧ��T1ʱ��ƽ�ⳣ����T2ʱ��С
C.�� T1��T2����S��С
D.����A��ķ�Ӧ��ϵ��T1�䵽T2���ﵽƽ��ʱ![]() ����
����
����T1�¶�ʱ����1.00molCO��2.00molH2����1.00L�����ܱ������У���ַ�Ӧ�ﵽƽ����������������ѹǿ��С����ʼʱ��һ�룬��ʱCO��ת����Ϊ______________��ƽ�ⳣ��Ϊ________________�������������
��2����һ�����ݵ��ܱ������з�����ӦCO(g)+2H2(g) ![]() CH3OH(g)���ڲ�ͬʱ��ⶨ�ĸ��ɷ����ʵ���Ũ�����±���
CH3OH(g)���ڲ�ͬʱ��ⶨ�ĸ��ɷ����ʵ���Ũ�����±���
ʱ�� | Ũ��(mol/L) | ||
c(CO) | c(H2) | c(CH3OH) | |
��0 min | 4.0 | 8.0 | 0 |
��10min | 3.8 | 7.6 | 0.2 |
��20min | 3.4 | 6.8 | 0.6 |
��30min | 3.4 | 6.8 | 0.6 |
��40min | 3.9 | 7.8 | 0.1 |
�� CO��ƽ����Ӧ����v(0min��10min)/ v(10min��20min)��________________��
�� ���ڵ�30minʱ�ı��˷�Ӧ�������ı�ķ�Ӧ����������______________��
���𰸡� �� AD 75% 12L2/mol2 1��2 �����¶�
��������(1)�ٸ������ȹ���ƽ��ֵ����֪T1��T2���ʴ�Ϊ������
��A.�������ȹ���ƽ��ֵ����֪T1��T2�������¶ȣ��״������ʵ�����С����ƽ�����淴Ӧ�����ƶ�������淴ӦΪ���ȷ�Ӧ��������ӦΪ���ȷ�Ӧ����A��ȷ��B���������ȹ���ƽ��ֵ����֪T1��T2�������¶ȣ��״������ʵ�����С����ƽ�����淴Ӧ�����ƶ�������ƽ�ⳣ����K(T1)��K (T2)����B����C.�� T1��T2�����������¶ȣ�ƽ�������ƶ�����������ʵ���������S����C����D�������¶�ƽ�������ƶ����ﵽƽ��ʱ![]() ����D��ȷ����ѡAD��
����D��ȷ����ѡAD��
���跴Ӧ��CO�����ʵ���Ϊx��
CO(g)+2H2(g)CH3OH(g)
����(mol)��1 2 0
�仯(mol)��x 2x x
ƽ��(mol)��1-x 2-2x x
�����ѹǿ��С����ʼʱ��һ�룬˵����������ʵ������ԭ����һ�룬��(1-x)+(2-2x)+x=1.5�����x=0.75mol��CO��ת����=![]() ��100%=75%���������Ϊ1L�����ƽ�ⳣ��K=
��100%=75%���������Ϊ1L�����ƽ�ⳣ��K=![]() =12���ʴ�Ϊ��75%��12��
=12���ʴ�Ϊ��75%��12��
(2)��CO��ƽ����Ӧ����![]() =
=![]() =
=![]() ���ʴ�Ϊ��
���ʴ�Ϊ�� ![]() ��
��
���ɱ������ݿ�֪����20minŨ�Ȳ��ٱ仯����Ӧ�ﵽ��ƽ��״̬����30minʱ�ı���������ƽ�������ƶ���c(CO)��c(H2)��c(CH3OH)�ı仯���ֱ�Ϊ0.5 mol/L��1.0 mol/L��0.5 mol/L�����㷽��ʽ���ʲ�����Ϊ����ijһ����Ũ�ȣ�����ѹǿ��Ӧ������Ũ�ȶ�Ӧ����˵���ı�������������Ǵ�����Ҳ��������Ũ�Ⱥ�ѹǿ��ֻ���Ǹı���¶ȣ�����30min��40min֮�䷴Ӧ���ʱ�10min��20min�죬ֻ���������¶ȣ��ʴ�Ϊ�������¶ȡ�


 ��Կ���Ծ�ϵ�д�
��Կ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��CO2��ת���������ܹ��ܺõļ�������ЧӦ������������Ľ���ṩ��һ���ܺõķ������������л��ϳɵķ�ʽ���Ժϳɴ��ᡢ�״��ȣ�������ʽת��Ϊ̼���λ���̼�����Ρ�
I.(1)������Ҳ����̼���Σ�������Na2CO3�����ϸ�ʱ��pH�ɸߴ�10.5���������ӷ���ʽ���������ʼ��Ե�ԭ��:_______________������ʯ��(CaSO4��5H2O)����ʹ�������Խ��ͣ�ԭ����(�û�ѧ�������)_____________________________��
(2)��������20mL0.1mol/LNa2CO3��Һ����μ���40mL0.1mol/LHCl��Һ����Һ�к�̼Ԫ�صĸ�����(CO2���ݳ�δ����)���ʵ�������(����)����ҺpH�仯�IJ��������ͼ��ʾ���ش���������:
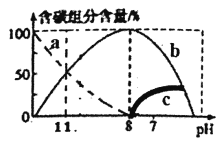
����ͬһ��Һ�У�H2CO3��HCO3-��CO32-_____(��ܡ����ܡ�)�������档
����Һ�и������ӵ����ʵ���Ũ�ȹ�ϵ��ȷ����Ϊ_______��
A.pH=11ʱ:c(Na+)>c(H2CO3)>c(CO32-)>c(OH-)>c(H+)
B.pH=11ʱ:c(HCO3-)>c(Cl-)
C.pH=7ʱ: c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)=c(H+)
D.pH=11ʱ: c(Na+)+c(H+)=3c(CO32-)+c(OH-)
�ۼ����̼���Ƶ�ˮ��ƽ�ⳣ��Ϊ________��
II.����ɱ��ͣ��������б��㷺Ӧ�á�
(1)��ij�¶���,CH3COOH(aq)��NaOH(aq)��Ӧ�ġ�H=-46.8kJ/mol����H2SO4(aq)��NaOH(aq)���к���Ϊ57.3kJ/mol����CH3COOH��ˮ��Һ�е���ġ�H=_________��
(2)��������ѧ���о�����������ϩ������Ϊԭ�ϡ��Ӷ����������ϳ������������¹��գ����������Ҵ�����ȩ���м��壬ʹ��Ʒ�ɱ����ͣ��������Ծ�������.��ϳɵĻ�����Ӧ���£� CH2=CH2��g��+CH3COOH(l) ![]() CH3COOC2H5(l) �÷�Ӧ������______��Ϊ������������ĺϳ����ʺͲ��ʣ����Բ�ȡ�Ĵ�ʩ��________(��д��һ��)��
CH3COOC2H5(l) �÷�Ӧ������______��Ϊ������������ĺϳ����ʺͲ��ʣ����Բ�ȡ�Ĵ�ʩ��________(��д��һ��)��
(3)��n(��ϩ)��n(����)���ϱ�Ϊ1�������£�ij�о�С���ڱ��ֲ�ͬѹǿ�½���������ͬʱ������������IJ������¶ȵı仯�IJⶨʵ�飬ʵ������ͼ��ʾ��

�ش���������:
���¶���60��80�淶Χ�ڣ���ϩ�����������ϳɷ�Ӧ�����ɴ�С��˳����______[��v(P1).v(P2)��v(P3)�ֱ��ʾ��ͬѹǿ�µķ�Ӧ����]��
��a��b��c������ϩ��ת���ʴӴ�С˳��______��
��P1�����������IJ���60�桫90��ʱ�������ߺ͵�ԭ����_______�����ݲⶨʵ���������������˵�����������___________(���ʵ�ѹǿ���¶�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.��������һ�����ڻ�ѧ��
B.���������Ӽ�ͨ�������������γɵĻ�ѧ���������Ӽ�
C.ֻ�н���Ԫ�غͷǽ���Ԫ�ػ���ʱ�����γ����Ӽ�
D.���ӻ������п��ܺ����ۼ������ۻ������в������Ӽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������������Ⱦ���ǣ� ��
��ú��ȼ�� �ڹ�ҵ���������ŷ� ��ȼ�ű��� �ܷɻ�������β�����ŷ�
A.ֻ�Т٢�
B.ֻ�Тڢ�
C.ֻ�Т٢ڢ�
D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ͬ�¶���CH3COOH��NH3H2O�ĵ��볣����ȣ�����10mLŨ��Ϊ0.1molL��1��CH3COOH��Һ�еμ���ͬŨ�ȵİ�ˮ���ڵμӹ����У�������
A.ˮ�ĵ���̶�ʼ������
B.c��NH4+����c��NH3H2O��ʼ�ռ�С
C.c��CH3COOH����c��CH3COO��֮��ʼ�ձ��ֲ���
D.�����백ˮ�����Ϊ10mLʱ��c��NH4+��=c��CH3COO����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڲⶨθ����ø����ʱ������Һ��pH��10����2�Ĺ����У�θ����ø�Ļ��Խ� �� ��
A���������� B�������� C���Ƚ����� D��û�б仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʳ��Ʒ�Խ�������ͥ�����Σ�������������ʲ����ڶ�Ʒ���ǣ� ��
A.����
B.����
C.������
D.�̲�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽���������ǣ� ��
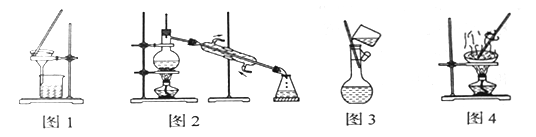
A. ͼ1��ʾΪ��ȥ������ˮ����ɳ�ķ���
B. ͼ2��ʾΪ��ȡ����ˮ�ķ���
C. ͼ3��ʾΪϡ��Ũ����ķ���
D. ͼ4��ʾΪ�����Ȼ�����Һ���Ȼ��ƾ���ķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���߷��Ӳ���PET������֬��PMMA�ĺϳ�·������ͼ:
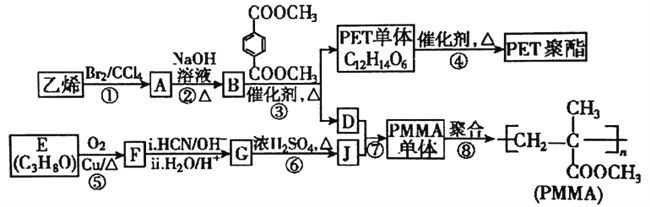
��֪:
I.RCOOR+R "OH![]() RCOOR "+ROH (R.R'��R"��������)
RCOOR "+ROH (R.R'��R"��������)
II.  (R��������)��
(R��������)��
(1)PMMA����Ľṹ��ʽΪ_______��PET�����еĹ���������Ϊ________��
(2)��Ӧ�ݵķ�Ӧ������________����Ӧ�ڵĻ�ѧ����ʽΪ_________��
(3)����Ӧ�ܵõ���ijһ����״����ۺ϶�Ϊn�������۷�Ӧ����ȥ��С��������___������
(4)PMMA�����ж���ͬ���칹�壬ij���칹��K�����������ʣ��ٲ��ܷ���������Ӧ�ڲ���ʹ��ˮ��ɫ�۷�����û�л�״�ṹ�ܺ˴Ź��������������Ϊ3:1�����ַ壬��K�Ľṹ��ʽΪ:__________����һ���칹��H����ȩ�����ǻ���̼̼˫������ͭ������������������������һ�֣���H�����Ľṹ����___��(�����������칹�Ϳռ��칹)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com