
| A. | 分液、过滤、蒸馏 | B. | 过滤、蒸馏、分液 | C. | 分液、蒸馏、过滤 | D. | 蒸馏、过滤、分液 |
科目:高中化学 来源: 题型:选择题
| A. | C(s)+H2O(g)?CO(g)+H2(g) 加入大量C固体,V正 增大,V逆 减小 | |
| B. | Zn(s)+HCl(aq)═ZnCl2(aq)+H2(g),使用纯锌比粗锌反应速率快 | |
| C. | 对于反应H2(g)+I2(g)?2HI(g),恒温恒容充入Ne,容器内压强增大,V正、V逆 均增大 | |
| D. | 对于反应2SO2(g)+O2(g)═2SO3(g)当升高温度V正、V逆 都加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅溶于水所得溶液能使紫色石蕊溶液变为红色 | |
| B. | 二氧化硅是非金属化物,易溶于水 | |
| C. | 二氧化硅与石棉(CaO•3MgO•4SiO2)都是硅盐酸 | |
| D. | 二氧化硅与硅酸都能溶于烧碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
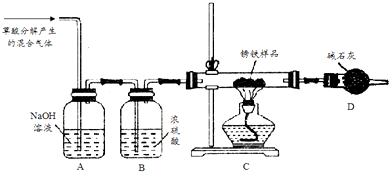
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
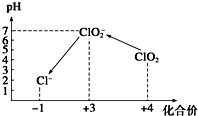 ClO2气体是一种常用的消毒剂,近几年我国用ClO2代替氯气对饮用水进行消毒.
ClO2气体是一种常用的消毒剂,近几年我国用ClO2代替氯气对饮用水进行消毒.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
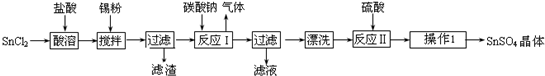
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用润湿的pH试纸测稀酸溶液的pH,测定值偏小 | |
| B. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏大 | |
| C. | 滴定前滴定管内有气泡,终点读数时无气泡,所测体积偏小 | |
| D. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na→NaOH→Na2CO3→NaCl | B. | Cu→CuO→Cu (OH)2→CuCl2 | ||
| C. | Mg→MgCl2→Mg(OH)2→MgSO4 | D. | Fe→FeCl2→Fe(OH)2→Fe(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com