
25℃时,下列各溶液中有关微粒物质的量浓度关系正确的是
A.0.1 mol·L-1Na2S溶液中:2c(Na+) =c(S2-)+c(HS-) +c(H2S)
B.pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合:c(Na+)+ c(H+)= c(OH-)+c(CH3COO-)
C.0.1 mol·L-1盐酸与0.1 mol·L-1K2CO3溶液等体积混合:c(K+) >c(Cl-)>c(HCO3-)>c(OH-)>c(H+)
D.0.1 mol·L-1NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(NH4+)>c(SO42-)>c(OH-) =c(H+)
BC
【解析】
试题分析:A.0.1 mol·L-1Na2S溶液中,根据物料守恒可得:c(Na+) =2c(S2-)+2c(HS-) +2c(H2S).错误;B.pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,根据电荷守恒可得:c(Na+)+ c(H+)= c(OH-)+c(CH3COO-),正确;C.0.1 mol·L-1盐酸与0.1 mol·L-1K2CO3溶液等体积混合。恰好发生反应:K2CO3+HCl= KCl +KHCO3,溶液是KCl、KHCO3等物质的量的混合物,由于HCO3-水解消耗水电离产生的H+,破坏了水的电离平衡,当最终达到平衡时c(OH-)>c(H+),但是盐水解的程度是微弱的,主要以盐电离产生的离子存在,所以离子浓度关系是:c(K+) >c(Cl-)>c(HCO3-)>c(OH-)>c(H+),正确;D.0.1 mol·L-1NH4HSO4溶液中滴加NaOH至溶液恰好呈中性,则NH4+水解消耗,SO42-无变化,所以离子浓度关系是:c(Na+) >c(SO42-)>c(NH4+)>c(OH-) =c(H+),错误。
考点:考查溶液中微粒物质的量浓度大小关系的判断的知识。


科目:高中化学 来源:2014-2015江苏省盐城市高二12月月考化学试卷(解析版) 题型:选择题
4.下列电离方程式中正确的是
A.NaHCO3溶于水:NaHCO3=Na++H++CO32-
B.NaHSO4熔化:NaHSO4=Na++H++SO42-
C.HF溶于少量水中:2HF H++HF2一
H++HF2一
D.(NH4)2 SO4溶于水:(NH4)2 SO4=2NH4++SO42一
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都郫县高三第二次阶诊断性考试理综化学试卷(解析版) 题型:填空题
(18分)A、B、C、D、E都是周期表中前四周期的元素。已知A原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大。B的基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数相同,B位于元素周期表的S区。C元素原子的外围电子层排布式为nsn—1npn—1。D原子M能层为全充满状态,且最外层无成对电子,E的化合物种类最多。请回答下列问题:
(1)写出D基态原子的电子排布式 ;
(2)A的常见氢化物AH3 的VSEPR模型为
(3)已知A和C形成的化合物X中每个原子的最外层均为8电子稳定结构,则X的化学式为 ,X是一种超硬物质,耐磨损、抗腐蚀能力强,
推测X的晶体类型为 。
(4)E的最高价氧化物的结构式为 中心原子的杂化方式为 。
(5)B的单质与A的最高价含氧酸的稀溶液反应,能将A还原至最低价态,写出该反应的化学方程式 。
(6)TiO2的天然晶体中,最稳定的一种晶体结构如下图,黑球表示 原子。

(7)二茂铁(C5H5)2Fe是Fe2+与环戊二烯基离子结合形成的小分子化合物,该化合物中Fe2+与环戊二烯基离子之间以 (填“离子键”、“金属键”、“配位键”、“氢键”、“范德华力”)相结合。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:选择题
如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1 mol,水的质量为100 g.。
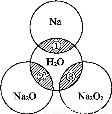
下列说法正确的是
A.Na2O2晶体中阴阳离子数目之比为1∶1
B.反应③最多能产生0.05 mol O2
C.反应①的离子方程式为Na+2H2O==Na++2OH-+H2↑
D.①、②、③充分反应后所得溶液的质量分数从大到小的顺序为①>②>③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:实验题
(14分)某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
Ⅰ.测定过氧化氢的含量
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL_______(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为________。
(3)判断滴定到达终点的现象是_________________________。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为____________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
实验内容 | 实验方法 | 实验现象 |
验证氧化性 | ||
验证不稳定性 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:选择题
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价绝对值相等,Z的核电荷数是Y的2倍,W最外层电子数是最内层电子数的3倍.下列说法正确的是
A.微粒半径:Z2+>W2->R-
B.对应氢化物的稳定性:W>R
C.W与X、W与Z形成的化合物晶体类型相同
D.Y的最高价氧化物对应的水化物是弱酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:选择题
下列有关化学用语表示错误的是
A.HCN的结构式:H-C≡N
B.HClO的电子式为:
C.HOCH2COOH缩聚物的结构简式:
D.2-氯甲苯的结构简式:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.用稀硫酸去除铜器表面的Cu2(OH)2CO3:Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O
B.用稀硝酸去除试管内壁的银镜:Ag+NO3-+2H+=Ag++NO2↑+H2O
C.向AlCl3溶液中加入氨水制Al(OH)3:Al3++3OH-=Al(OH)3↓
D.向FeI2溶液中加入盐酸和过量的H2O2:2I-+H2O2+2H+=I2+2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏常州市高三第一次调研试卷化学试卷(解析版) 题型:选择题
某芳香化合物的分子式为C8H8Cl2O2,其分子结构中有三种不同化学环境的氢,它们的数目之比为6︰1︰1,且分子中的Cl原子皆形成C-Cl键,则其可能的结构有(不考虑O与O相连接)
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com