
【题目】下列有关盐类水解的相关描述中,不正确的是( )
A.中国古代利用明矾溶液清除铜镜表面的铜锈
B.![]() 溶液中:
溶液中:![]()
C.0.1 mol/L.醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后的溶液中:![]()
D.物质的量浓度相等的①![]() ;②
;②![]() ;③
;③![]() 三种溶液中,pH值由大到小的顺序为②>③>①
三种溶液中,pH值由大到小的顺序为②>③>①
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
【题目】叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成。
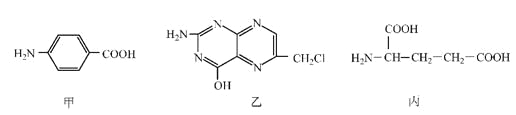
(1)甲中显酸性的官能团是_______________(填名称)。
(2)下列关于乙的说法正确的是__________________(填序号)。
a.分子中碳原子与氮原子的个数比是7:5 b.属于芳香族化合物
c.既能与盐酸又能与氢氧化钠溶液反应 d.属于苯酚的同系物
(3)丁是丙的同分异构体,且满足下列两个条件,丁的结构简式为________________。
a.含有![]() b.在稀硫酸中水解有乙酸生成
b.在稀硫酸中水解有乙酸生成
(4)甲可以通过下列路线合成(分离方法和其他产物已经略去):
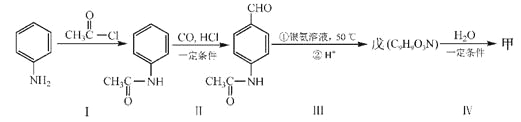
①步骤I的反应类型是______________________。
②步骤I和Ⅳ在合成甲过程中的目的是____________________。
③步骤Ⅳ反应的化学方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:FeCl3(aq)+3KSCN(aq)![]() 3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是
3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是
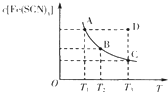
A.A点与B点相比,A点的c(Fe3+)大
B.加入KCl固体可以使溶液由D点变到C点
C.反应处于D点时,一定有υ(正)<υ(逆)
D.若T1、T2温度下的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组以乙烯等为主要原料合成药物普鲁卡因:
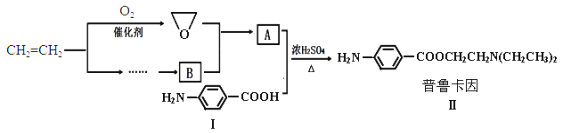
已知:![]() ,
,![]()
(1)对于普鲁卡因,下列说法正确的是___。
a.一个分子中有11个碳原子
b.不与氢气发生加成反应
c.可发生水解反应
(2)化合物Ⅰ的分子式为___,1mol化合物Ⅰ能与___molH2恰好完全反应。
(3)化合物Ⅰ在浓H2SO4和加热的条件下,自身能反应生成高分子聚合物Ⅲ,写出Ⅲ的结构简式___。
(4)请用化学反应方程式表示以乙烯为原料制备B(无机试剂任选)的有关反应,并指出所属的反应类型___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】比较纯碱的两种工业制法,正确的是
选项 | 项目 | 氨碱法 | 联合制碱法 |
A. | 原料 | 食盐、氨气、生石灰 | 食盐、氨气、二氧化碳 |
B. | 可能的副产物 | 氯化钙 | 氯化铵 |
C. | 循环物质 | 氨气、二氧化碳 | 氨气、氯化钠 |
D. | 评价 | 原料易得、产率高 | 设备简单、能耗低 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)元素Zn位于元素周期表的________族、________区;基态Zn原子价层电子的电子排布图(轨道表示式)为________。
(2)基态Zn原子核外电子占据最高能层的符号是________,占据该能层电子的电子云轮廓图形状为________形。
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成,第一电离能![]() __________
__________![]() (填“大于”或“小于”)。原因是________________。
(填“大于”或“小于”)。原因是________________。
(4)光催化还原![]() 制备
制备![]() 反应中,带状纳米
反应中,带状纳米![]() 是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________________。
是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
a | |||||||||||||||||
b | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o | p |
(1)在周期表中,与元素b的化学性质最相似的邻族元素是________(填写以上表中字母对应的元素符号),该元素基态原子核外M层电子的自旋状态________(填“相同”或“相反”)。
(2)元素As与________同族(填写以上表中字母对应的元素符号),其简单气态氢化物的稳定性由大到小的顺序是________。
(3)基态ρ原子成为阳离子时首先失去________轨道电子,基态![]() 的最外层电子排布式________。
的最外层电子排布式________。
(4)i的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式为________________。
(5)下列关于上图表中元素说法正确的是________(填序号)。
①未成对电子数最多的元素是O
②元素的电负性强弱;![]()
③元素的第一电离能:![]()
④简单离子半径:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在容积恒为2.0L的容器中,Fe和CO2发生如下反应: CO2(g) + Fe(s) ![]() FeO(s) + CO(g),若起始时向容器中加入1mol CO2,5.0 min后,容器内气体的相对平均分子量为32,则这段时间内ν(CO2)=_____________。
FeO(s) + CO(g),若起始时向容器中加入1mol CO2,5.0 min后,容器内气体的相对平均分子量为32,则这段时间内ν(CO2)=_____________。
①下列说法不正确的是_______
a 当混合气体的密度不变时说明反应达到了平衡
b 混合气体的平均相对分子质量不变时说明反应达到了平衡
c 平衡后移除二氧化碳时,正反应速率一直减小直至建立新的平衡
d 平衡后缩小容器的体积,正逆反应速率不变,平衡不移动
②待反应达到平衡后再充入一定量的二氧化碳,平衡向_________移动(选填“正向”、 “逆向”、或“不”),二氧化碳的转化率________(填“增大”,“减小”或“不变”),CO的物质的量____(选填“增大”,“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。电解质溶液为KOH溶液,电池反应为:Cd +2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2,下列有关镍镉电池的说法正确的是
Cd(OH)2+2Ni(OH)2,下列有关镍镉电池的说法正确的是
A. 充电过程是化学能转化为电能的过程
B. 充电时阳极反应为Cd(OH)2+2e—="=" Cd + 2OH-
C. 放电时电池内部OH - 向正极移动
D. 充电时与直流电源正极相连的电极上发生Ni(OH)2转化为NiO(OH)的反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com