
【题目】现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示。则X是( )

A. 水
B. 澄清石灰水
C. 纯碱溶液
D. 稀盐酸
【答案】C
【解析】A、向盐酸和CaCl2的混合溶液中加入水时,溶液的酸性减弱,但是不能达到7,也就是说加入水稀释时溶液仍然显酸性,A错误;B、向盐酸和CaCl2的混合溶液中加入澄清石灰水时,盐酸能和氢氧化钙反应,随着反应的进行溶液的酸性减弱,pH升高,当恰好完全反应时溶液显中性,继续加入石灰水时溶液的pH升高,不会出现平行于X轴的线段,B错误;C、向盐酸和CaCl2的混合溶液中加入纯碱溶液时,碳酸钠能和盐酸反应,随着反应的进行溶液的酸性减弱,pH升高,当恰好完全反应时溶液显中性,继续加入碳酸钠时,碳酸钠又和氯化钙反应碳酸钙沉淀和显中性的氯化钠,在碳酸钠和氯化钙反应的过程中溶液的pH不变,当氯化钙完全反应后,再加入碳酸钠时,溶液的pH又升高,C正确;D、向盐酸和CaCl2的混合溶液中加入稀盐酸时,溶液仍然显酸性,D错误,答案选C。


科目:高中化学 来源: 题型:
【题目】从香荚兰豆中提取的一种芳香化合物,其分子式为C8H8O3,遇FeCl3溶液会呈现特征颜色,能发生银镜反应。该化合物可能的结构简式是( )
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关性质的比较,不能用元素周期律解释的是( )
A.碱性:KOH>NaOH
B.金属性:Na>Mg
C.稳定性:HF>CH4
D.酸性:HF<HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)①氯胺(NH2Cl)的电子式为_______。
②工业上可利用Cl2和NH3反应制备氯胺,该反应的化学方程式为_______。
(2)一定条件下,不同物质的量的CO2与不同体积的1.0 mol·L-1 NaOH溶液充分反应放出的热量如下表所示:
反应序号 | CO2的物质的量/mol | NaOH溶液的体积/L | 放出的热量/kJ |
1 | 0.5 | 0.75 | x |
2 | 1.0 | 2.00 | y |
该条件下CO2与NaOH溶液反应生成NaHCO3的热化学反应方程式为__________。
(3)用焦炭还原NO的反应为:2NO(g) + C(s) ![]() N2(g) + CO2(g),向容积均为1 L的甲、乙、丙三个恒温(反应温度分别为400 ℃、T ℃、400 ℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g) + CO2(g),向容积均为1 L的甲、乙、丙三个恒温(反应温度分别为400 ℃、T ℃、400 ℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
t/min | 0 | 40 | 80 | 120 | 160 |
n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(NO)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
n(NO)(丙容器)/ml | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
①甲容器中,0~40 min内用NO的浓度变化表示的平均反应速率v(NO)=_________。
②该反应的ΔH___0 (填“>”或“<”)。
③丙容器达到平衡时,NO的转化率为___________。
(4)常温下,在NH4HCO3溶液中,c(NH4+)________c(HCO3-) (填“>”、“<”或“=”);反应NH4++HCO3-+H2O ![]() NH3·H2O+H2CO3的平衡常数K=__________。(已知常温下,NH3·H2O的电离平衡常数Kb = 2×10-5,H2CO3的电离平衡常数Ka1 = 4×10-7,Ka2 = 4×10-11)
NH3·H2O+H2CO3的平衡常数K=__________。(已知常温下,NH3·H2O的电离平衡常数Kb = 2×10-5,H2CO3的电离平衡常数Ka1 = 4×10-7,Ka2 = 4×10-11)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。其部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解产生大量白雾 ②易分解:SO2Cl2=SO2↑+Cl2↑ |
回答下列问题:
I.实验室合成硫酰氯需要先制取干燥氯气,制备干燥纯净的氯气所用仪器如下图:

(1)上述仪器的连接顺序是:e接__, 接 , 接 , 接 (按气流方向,用小写字母表示)。
II.催化合成硫酰氯的实验装置如下图 (夹持仪器已省略):

(2)仪器B冷却水的进口为________(填“a””或“b”),活性炭的作用是________。
(3)装置D除干燥气体外,另一作用是_______________。若缺少D,则硫酰氯会水解,该反应的化学方程式为________________。
(4)某同学建议将收集器A放在冰水中冷却,你认为该同学的建议是否合理,为什么?______________________________
(5)C处U形管中碱石灰的作用是__________________________________________。
III.在氯磺酸中加入四氯化锡加热煮沸,使氯磺酸分解,可用于制取少量硫酰氯。化学方程式为:2ClSO3H = H2SO4+SO2Cl2,此法得到的产品中混有硫酸。
(6)①从分解产物中分离出硫酰氯的方法是________。②请设计实验方案检验产品中硫酸的存在(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年朝鲜进行氢弹实验.引起国际社会的极大关注。下列关于31H的说法正确的是( )
A. 质量数是1B. 质子数是2C. 中子数是2D. 电子数是3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、下图是维生素A的分子结构:
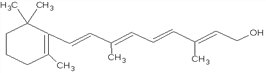
(1)维生素A的分子式是__________________,1mol维生素A最多能与____________mol溴发生加成反应。
(2)根据要求写出下列有机物的结构简式或者系统命名:
CH3CH(CH3)C(CH3)2CH2CH3 :__________________________________.
2﹣甲基﹣2﹣丁烯:________________________________________________.
Ⅱ、人们对苯及芳香烃的认识有一个不断深化的过程。
(3)已知分子式为C6H6的结构有多种,其中的两种见图(Ⅰ)、(Ⅱ):
![]()
①这两种结构的区别表现在:
定性方面(即化学性质方面):Ⅰ不能_______(填字母,下同)而Ⅱ不能________.
A.被酸性高锰酸钾溶液氧化 B.与溴的四氯化碳溶液发生加成反应
C.与溴在催化剂作用下发生取代反应 D.与氢气发生加成反应
定量方面:1molC6H6与H2加成时:Ⅰ需________mol,而Ⅱ需_______mol.
②今发现C6H6还有另一种如图立体结构![]() :该结构的二氯代物有________种.
:该结构的二氯代物有________种.
③根据苯的分子结构,可以推测苯的性质比较稳定,容易发生取代反应,不易发生加成和氧化反应。写出苯与硝酸在催化剂作用下反应的化学方程式____________________________
(4)已知萘的结构简式为 ![]() ,下列关于萘的说法正确的是_______(填编号)
,下列关于萘的说法正确的是_______(填编号)
A.萘的分子式为C10H10 B.1mol萘能与6molH2发生加成反应
C.萘分子中所有原子在同一平面上 D.一溴代萘只有两种同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com