
【题目】如图所示是过氧化氢(H2O2)分子的空间结构示意图。

(1)写出过氧化氢分子的电子式________。
(2)下列关于过氧化氢的说法中正确的是(填序号)______________。
①分子中有极性键 ②分子中有非极性键 ③氧原子的轨道发生了sp2杂化 ④O—O共价键是p—pσ键 ⑤分子是非极性分子
(3)过氧化氢分子之间易形成氢键,该氢键的表示式是____________。
(4)过氧化氢难溶于二硫化碳,主要原因是_________________;过氧化氢易溶于水,主要原因是_________________。
(5)过氧乙酸也是一种过氧化物,它可以看作是过氧化氢分子中的一个氢原子被乙酰基(CH3CO)取代的产物,是一种常用的杀菌消毒剂。在酸性条件下过氧乙酸易发生水解反应生成过氧化氢。
①写出过氧乙酸发生水解反应的化学方程式(有机物用结构简式表示):________________________。
②过氧乙酸用作杀菌消毒剂的原因是____________________________。
【答案】(1) ![]()
(2)①②
(3)O—H…O—
(4)H2O2分子是极性分子,CS2分子是非极性分子H2O2分子与H2O分子之间形成氢键
(5)①![]() +H2O―→CH3COOH+H2O2
+H2O―→CH3COOH+H2O2
②过氧乙酸分子中有O—O键,有强氧化性
【解析】在H—O—O—H分子中,H—O键是极性键,O—O键是非极性键。由于H2O2分子具有图中所示的空间结构,所以H2O2分子是极性分子。借助H2O分子中氧原子发生的原子轨道杂化可知,H2O2分子中氧原子的原子轨道杂化方式是sp3,所以O—O共价键不是p-pσ健。H—O—O—H分子中的O—H键决定了H2O2分子之间存在氢键。H2O2分子是极性分子,CS2分子是非极性分子,H2O2分子和CS2分子之间不能形成氢键,H2O2和CS2不发生化学反应,所以过氧化氢难溶于二硫化碳,可用“相似相溶”原理解释。H2O2分子和H2O分子中都含有O—H键,所以H2O2分子与H2O分子之间可形成氢键,氢键的形成能增大物质的溶解度。


科目:高中化学 来源: 题型:
【题目】两分子乙炔反应得到乙烯基乙炔(CH2===CH—C≡CH),该物质是合成橡胶的重要原料,下列关于该物质的判断错误的是( )
A.该物质既是H2C===CH2的同系物,又是HC≡CH的同系物
B.该物质既能使酸性KMnO4溶液褪色,又能使溴水褪色
C.该物质与足量的H2加成后,只能生成一种物质
D.该物质经加成、加聚反应后的产物是氯丁橡胶(![]() )的主要成分
)的主要成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.某金属元素气态基态原子的逐级电离能的数值分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X3+
B.粗硅 ![]() SiCl4
SiCl4 ![]() Si均能一步实现
Si均能一步实现
C.33gCH≡C﹣CH=CH﹣CH3中所含的π键数、12g石墨中所含的碳碳键数均为1.5mol
D.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+ , 可能含有K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水中,水分子可彼此通过氢键形成(H2O)n的小集团。在一定温度下(H2O)n的n=5,每个水分子被4个水分子包围着形成四面体。(H2O)n的n=5时,下列说法中正确的是 ( )
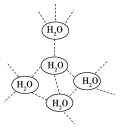
A.(H2O)n是一种新的水分子
B.(H2O)n仍保留着水的化学性质
C.1 mol(H2O)n中有2个氢键
D.1 mol(H2O)n中有4 mol氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》中“烧酒”条目写道:“自元时始创其法,用浓酒和糟人甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”文中所用之“法”是指 ( )
A.蒸馏B.渗析C.萃取D.过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定已变质的过氧化钠的纯度,设计如下图所示的实验;Q为一具有良好的弹性气球,称取一定量的样品放于其中,按图安装的实验装置打开分液漏斗的活塞,将稀H2SO4滴入气球中.请填空:
(1)Q内发生反应生成种气体,其中的反应有个氧化还原反应.
(2)为测定反应生成气体的总体积,滴稀H2SO4前必须关闭(填K1、K2或K3 , 下同) , 打开 .
(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2 , 再缓缓打开K1 , 这时可观察到的现象是 .
(4)导管a的作用是 .
(5)b中装的固体试剂是 , 为何要缓缓打开K1 .
(6)实验结束时量筒I中有x mL水,量筒II中收集到y mL气体,则过氧化钠的纯度是(体积折算到标准状况).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种高容量的固态锂电池以锂超离子固态导体(组成为Li30GeP2S12)为电解质,该锂电池能在﹣100℃至100℃之间的超宽温度范围内工作.下列说法不正确的是( )
A.Li的原子结构示意图为 ![]()
B.原子半径:P>S
C.酸性:H3PO4<H2SO4
D.Li、Ge、P、S都属于短周期元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1 mol·L-1的某一元酸HA在水中有0.1%发生电离,回答下列各问题:
(1)HA的电离平衡常数K=_____________。
(2)升高温度时,K将_____________(填“增大”、“减小”或“不变”)。(3)由HA电离出的c(H+)约为水电离出的c(H+)的_____________倍。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com