
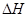 的绝对值均正确)( )
的绝对值均正确)( )| A.C2H5OH(l)+3O2(g)==2CO2(g) +3H2O(g);△H=" —1367.0" kJ/mol(燃烧热) |
| B.NaOH(aq) + HCl(aq) ="=" NaCl(aq) + H2O(l);△H= —57.3kJ(中和热) |
| C.S(s) + O2(g) ="=" SO2(g);△H= —269.8kJ/mol(反应热) |
| D.2NO2==O2+2NO;△H= +116.2kJ/mol(反应热) |
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ? 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。
? 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。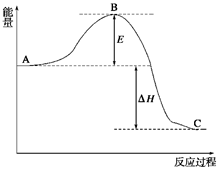
 v(O2)= mol/(L·min)、v(SO3)= mol/(L·min);
v(O2)= mol/(L·min)、v(SO3)= mol/(L·min); ?SO2(g) ΔH=-296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH 。
?SO2(g) ΔH=-296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H—Cl→H + Cl | B.H + H→H—H |
| C.Zn + H2SO4 = ZnSO4 + H2 ↑ | D.HCl+ NaOH =" NaCl+" H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
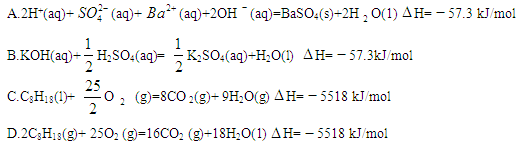
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(1)DH=+28.6kJ/mol |
| B.NaOH(aq)+HCL(aq) = NaCl(aq)+H2O(1)DH=-28.6kJ/mol |
| C.NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(1)DH=+57.2kJ/mol |
| D.NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(1)DH=-57.2kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题



 溶液的浓度应为 mol/L。
溶液的浓度应为 mol/L。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com