
A、 排水法收集NO |
B、 实验室制取并收集氧气 |
C、 除去氯气中的HCl |
D、 分离碘酒中的碘与酒精 |
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
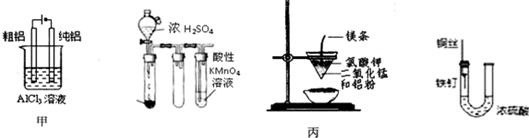
| A、用甲图装置电解精炼铝 |
| B、乙图中酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C、丙图装置可制得金属锰,用同样的装置可制得金属铬 |
| D、丁图装置中的铁钉几乎没被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性:Na2CO3<NaHCO3 |
| B、相同条件下,溶于水溶液的碱性:Na2CO3<NaHCO3 |
| C、常温下,在水中的溶解度:Na2CO3>NaHCO3 |
| D、相同条件下,与稀盐酸反应的快慢:Na2CO3<NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸、碱一定含氢,盐一定不含氢 |
| B、酸、碱、盐可能都不含金属元素 |
| C、碱、盐可能含氧,酸一定含氧 |
| D、盐一定含金属元素,酸、碱不一定含金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应SiO2+3C═SiC+2CO中,氧化剂与还原剂的物质的量之比为1:2 |
| B、向蔗糖中加入浓硫酸,蔗糖变黑,并有刺激性气味,说明浓硫酸具有脱水性和强氧化性 |
| C、浓硫酸、浓硝酸在加热条件下都能将木炭氧化为二氧化碳 |
| D、铁粉与足量稀硝酸反应时,氧化剂与还原剂的物质的量之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
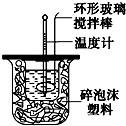 如图装置测定中和热的实验步骤如下:
如图装置测定中和热的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:
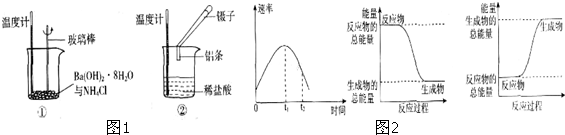
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com