
【题目】铁是一种应用广泛的金属。下列有关铁的说法错误的是
A.铁与盐酸反应生成氯化铁与氢气B.常温下,铁在浓硫酸中会发生钝化
C.铁在氧气中燃烧生成四氧化三铁D.铁是一种银白色金属
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列排列顺序正确的是
①热稳定性:H2O>HF>H2S ②离子半径:O2->Na+>Mg2+
③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力:OH->CH3COO->Cl-
A. ①③ B. ②④ C. ①④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:NaHSO4在水中的电离方程式为NaHSO4=Na++H++SO42﹣
(1)常温下,pH=5的NaHSO4溶液中水的电离程度pH=9的NH3H2O中水的电离程度.(填“>”、“=”或“<”)
(2)等体积等物质的量浓度的NaHSO4与氨水混合后,溶液呈酸性的原因为 . (用离子方程式表示);若一定量的NaHSO4溶液与氨水混合后,溶液pH=7,则c(Na+)+c(NH4+)
2C(SO42﹣)(填“>”、“=”或“<”);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42﹣完全沉淀,则反应后溶液的pH7(填“>”、“=”或“<”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题: 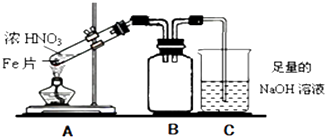
(1)甲同学完成了Fe、Cu分别与S、Cl2反应的实验,下列物质中不可能为甲同学实验得到的生成物是
A.FeCl3
B.FeCl2
C.CuCl2
D.FeS
(2)乙同学为验证Fe能和热的浓HNO3反应,设计了如图所示的实验装置,请说出装置B的作用: . 开始加热前(填“有”或“无”)明显现象.
(3)当乙同学实验结束时,铁完全溶解,试管液面上方为无色气体,试管上部为红棕色气体,此时丙同学用所得的溶液进行如下实验和探究:
①在所得的溶液中加入一小块Cu片,结果Cu片先逐渐溶解,并伴随其他现象,反应一段时间后不再溶解.丙同学依据反应现象得出Cu片溶解的原因可能是和过量的HNO3发生反应.他依据的反应现象是;该反应的离子方程式为 . 你认为Cu片溶解是否还有另一原因,若有请用化学方程式表示其理由:(若无此空不填)
②请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+ . 说明具体的操作和实验现象 .
③丙同学实验结束后加水稀释后得到溶液500mL,假设实验全过程硝酸只被还原成NO和NO2共0.02mol并测得溶液中Fe2+和Cu2+浓度均为0.02mol/L,则NO3﹣的物质的量浓度为mol/L.生成NO气体的体积为L(标准状况).
(4)本次探究实验用掉密度为1.5gcm﹣3质量分数为95%的浓硝酸3mL,超出实际参加反应的量其原因有(写出两点):①② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2L的密闭容器中充入7.6mol NO和3.8mol O2 , 发生如下反应:
①2NO(g)+O2(g)2NO2(g)
②2NO2(g)N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃.下列说法正确的是( )
A.前5min反应的平均速率v(N2O4)=0.36mol(Lmin)﹣1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2.0mol N2O4 , T1℃达到平衡时,N2O4的转化率为10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1molL﹣1 NaOH溶液滴定20mL 0.1molL﹣1CH3COOH溶液的滴定曲线如图所示.下列说法正确的是( )
A.点①所示溶液中:c(Na+)>c(CH3COO﹣)>c(CH3COOH)>c(H+)>c(OH﹣)
B.点②所示溶液中:c(Na+)+c(H+)=c(CH3COO﹣)+c(CH3COOH)+c(OH﹣)
C.点③所示溶液中:c(CH3COO﹣)>c(Na+)>c(OH﹣)>c(H+)
D.在整个滴定过程中:溶液中 ![]() 始终不变
始终不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①标准状况下,0.2 mol任何物质的体积均为4.48 L
②若1 mol气体的体积为22.4 L,则它一定处于标准状况下
③标准状况下,1 LCO和1 L H2O的物质的量相同
④标准状况下,1 g H2和14 g N2的体积相同
⑤28 g CO的体积为22.4 L
⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑦在同温同体积时,气体物质的物质的量越大,则压强越大
⑧同温同压下,气体的密度与气体的相对分子质量成正比
A.①②③④
B.②③⑥⑦⑧
C.④⑦⑧
D.⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如右图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )![]()
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性W比Z弱
C.Y的气态氢化物的稳定性较Z的弱
D.四种元素的单质中,Z的熔、沸点最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A.CO2的比例模型: ![]()
B.氢氧根离子的电子式: ![]()
C.氯原子的结构示意图: 
D.中子数为146,质子数为92的铀(U)原子 ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com