
【题目】在硝酸铵分解反应中,生成的含氮产物中仅有氮气和硝酸两种,其中被氧化的氮元素和被还原的氮元素物质的量之比为( )
A. 5:3 B. 1:1 C. 5:4 D. 3:5
科目:高中化学 来源: 题型:
【题目】关于硅及其化合物的叙述中,不正确的是( )
A.硅是良好的半导体材料
B.二氧化硅能与石灰石反应:SiO2+CaCO3 ![]() CaSiO3+CO2↑
CaSiO3+CO2↑
C.可以用焦炭还原二氧化硅生产硅:SiO2+2C ![]() Si+2CO↑
Si+2CO↑
D.水泥的主要成分是 Na2SiO3、CaSiO3 和 SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合处理“工业三废”,有利于保护环境,节约资源. 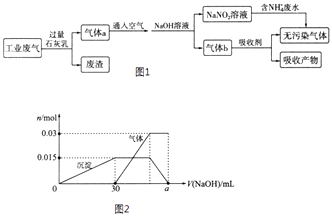
(1)为处理某工厂的工业废气(主要含N2、SO2、NO、CO,不考虑其他成分),设计了如图1流程:
已知:NO+NO2+2NaOH=2NaNO2+H2O;
2NO2+2NaOH=NaNO3+NaNO2+H2O.
①废渣的成分为(填化学式).
②通入空气不能过量,原因是 .
③吸收剂所吸收的气体主要是
④处理含NH4+废水时,发生反应的离子方程式为
(2)某无色工业废水中可能含有NH4+、Na+、Al3+、Cu2+、Cl﹣、SO42﹣、CO32﹣等离子中的几种离子.为确定其成分,设计如下实验:
a.取10mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,充分反应后过滤得到0.04mol白色沉淀,向滤液中加入AgNO3溶液无沉淀产生.
b.另取10mL该废水于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体,最后沉淀完全溶解.沉淀和气体的物质的量随加入NaOH溶液体积的变化关系如图2所示.(不考虑沉淀、气体的溶解和损失)
根据上述实验和图表数据:
①该废水中一定含有的离子有(填离子符号).
②实验室配制100mL所需浓度的NaOH溶液时,用到的玻璃仪器除烧杯、玻璃棒、量筒外,还需要(填仪器名称).
③图中a= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废旧铝铁合金(主要成分为Fe、Al、Fe2O3、Al2O3)制备纳米材料磁性Fe3O4粒子及副产物Al,制备流程图如图: 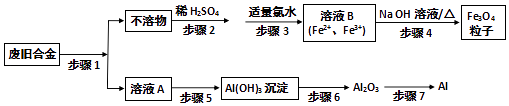
回答下列问题:
(1)步骤1中所用的试剂是 , 涉及的化学反应中属于氧化还原反应的化学方程式为
(2)步骤3中反应的离子方程式为 .
(3)步骤5可选用的试剂或操作最合理的是(填序号). a.NaOH溶液 b.氨水 c.盐酸 d.通入过量的CO2
(4)步骤7中每获得副产物Al 27g,转移的电子数目为 .
(5)下列关于磁性Fe3O4粒子的说法正确的是(填序号).
A.磁性Fe3O4粒子会产生丁达尔效应
B.磁性Fe3O4粒子的化学性质与原来的Fe3O4完全不同
C.磁性Fe3O4粒子属于胶体分散系
D.磁性Fe3O4粒子能透过滤纸.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年8月12日,天津滨海新区爆炸事故确认有氰化钠(NaCN)、亚硝酸钠等,氰化钠毒性很强,遇水、酸会产生有毒易燃氰化氢(HCN)气体。氰化氢的沸点只有26 ℃,因此相当容易挥发进入空气,这就大大增加了中毒的风险。同时氰化钠遇到亚硝酸钠会发生爆炸。回答下列问题:
(1)写出氰化钠遇水产生氰化氢气体的离子方程式_________________________
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理。氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式________________________________。
(3)爆炸残留在废水中的CN-可以用Cr2O![]() 处理,拟定下列流程进行废水处理,
处理,拟定下列流程进行废水处理,
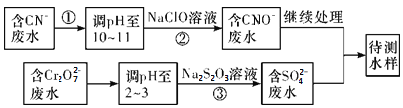
①上述处理废水流程中主要使用的方法是____________
a.混凝法 b.中和法 c.沉淀法 d.氧化还原法
②②中反应后无气体放出,该反应的离子方程式为_________________;
③步骤③中,每处理0.4 mol Cr2O![]() 时转移电子2.4 mol,该反应的离子方程式_________;
时转移电子2.4 mol,该反应的离子方程式_________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)能净化有毒废水中的氰化钠(NaCN),生成NaCl、CO2和N2 , 下列说法正确的是( )
A.被氧化的元素是氯元素
B.氧化产物与还原产物的物质的量之比为1:1
C.消耗1mol还原剂,转移5 mol电子
D.净化1 L含CN﹣1.04 mgL﹣1的废水,理论上需用2×l0﹣5mol C1O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下: 低温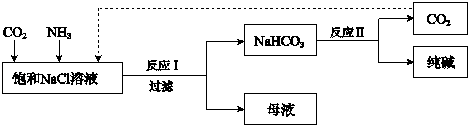
已知反应I为:NaCl+CO2+NH3+H2O ![]() NaHCO3↓+NH4Cl
NaHCO3↓+NH4Cl
(1)工业生产中,制备NH3的化学方程式是
(2)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO42﹣等离子. ①为得到纯净的饱和NaCl溶液,进行了如下操作.请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中 , 过滤;
c.向滤液中 , 过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液.
②步骤c中反应的离子方程式是 .
(3)反应II的化学方程式是 .
(4)制得的纯碱中含有少量NaCl.取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mL CO2 . 则样品中纯碱的质量分数是%(保留1位小数).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是 ( )
A.钠和冷水反应:Na+2H2O=Na++2OH+H2↑
B.金属铝溶于氢氧化钠溶液:Al+2OH=AlO2+H2
C.金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑
D.Fe(OH)3跟盐酸反应:OH+H+= H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为测定未知浓度的硫酸溶液,进行如下实验:用1.00mL待测硫酸溶液配制100mL稀H2SO4溶液;以0.14molL-1的NaOH溶液滴定上述稀H2SO4 25.00mL,滴定终止时消耗NaOH溶液15.00mL.
(1)该学生用0.14molL-1NaOH标准溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入指示剂.
B.用待测定的溶液润洗酸式滴定管
C.用蒸馏水洗干净滴定管
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2-3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
E.检查滴定管是否漏水
F.另取锥形瓶,再重复操作一次
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下
滴定管液面所在刻度
①滴定操作的正确顺序是(用序号填写) ( )→( )→D→( ) →A→( ) →( ) __________
②配制准确浓度的稀H2SO4溶液,必须使用的主要容器是 ______
③观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值 ______ (选填“偏高”“偏低”或“无影响”)
④计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果到小数点后二位)_____
⑤已知:含CH3COOH 1mol的醋酸溶液与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1;含HCl1mol 的盐酸与NaOH(aq)反应的ΔH=-55.6 kJ·mol-1。则CH3COOH在水溶液中电离的ΔH等于______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com