
以食盐为原料进行生产并综合利用的某些过程如下图所示。
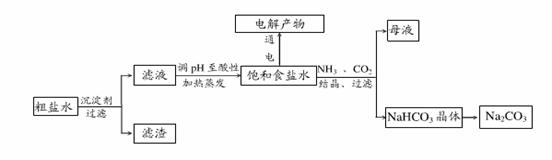
(1)除去粗盐中的 、
、 和
和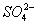 离子,加入下列沉淀剂的顺序是(填序号)____________________ 。 a.
离子,加入下列沉淀剂的顺序是(填序号)____________________ 。 a. 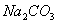 b.
b. 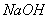 c.
c. 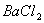
(2)将滤液的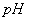 调至酸性除去的离子有___________________。
调至酸性除去的离子有___________________。
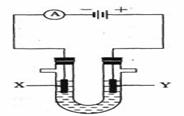
(3)人们习惯上把电解饱和食盐水的工业叫做氯碱工业。下图表示电解饱和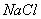 溶液的装置,X、Y是石墨棒。实验开始时,在两边同时各滴入几滴酚酞溶液,请回答以下问题:X极上的电极反应式是________________ ,在X极附近观察到的现象是________________;Y电极上的电极反应式是________________,检验该电极反应产物的方法是_______________
溶液的装置,X、Y是石墨棒。实验开始时,在两边同时各滴入几滴酚酞溶液,请回答以下问题:X极上的电极反应式是________________ ,在X极附近观察到的现象是________________;Y电极上的电极反应式是________________,检验该电极反应产物的方法是_______________
________________________________________________________________________。
电解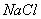 溶液的离子方程式是__________________________________________。
溶液的离子方程式是__________________________________________。
(4)若向分离出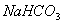 晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的气体,其化学式是 _____________________ 。
晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的气体,其化学式是 _____________________ 。
(5)某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
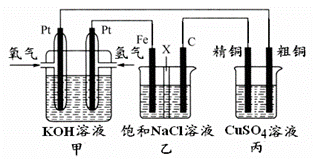
根据要求回答相关问题:
①通入氢气的电极为 (填“正极”或“负极”),负极的电极反应式为 。
②石墨电极为 (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,
_ 区(填“铁极”或“石墨极”)的溶液先变红。
③如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将 ,
填“增大”“减 小”或“不变”)。精铜电极上的电极反应式为
④若在标准状况下,有224m L氧气参加反应,则乙装置中铁电极上生成的气体在标况下
体积为 ;丙装置中阴极析出铜的质量为 。
科目:高中化学 来源: 题型:
被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O===NaBO2+4H2↑,下列说法中正确的是(NaBH4中H为-1价) ( )
A.NaBH4既是氧化剂又是还原剂
B.NaBH4是氧化剂,H2O是还原剂
C.硼元素被氧化,氢元素被还原
D.被氧化的元素与被还原的元素质量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
⑴烟气脱硫、脱硝的环境意义是 。
⑵选择性催化还原法的脱硝原理为:6NOx+4x NH3 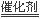 (3+2x)N2+6xH2O
(3+2x)N2+6xH2O
①上述反应中每转移3mol电子,生成标准状况下N2的体积为 L。
②已知:2H2(g)+O2(g) =2H2O (g) ΔH=-483.6 kJ·mol-1
N2(g)+3H2(g)=2NH3(g) ΔH=-92.4 kJ·mol-1
N2(g)+O2(g)=2NO(g) ΔH=-180.5kJ·mol-1
则反应6NO(g)+4NH3(g)=5N2(g)+6H2O(g)的ΔH= 。
⑶目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。
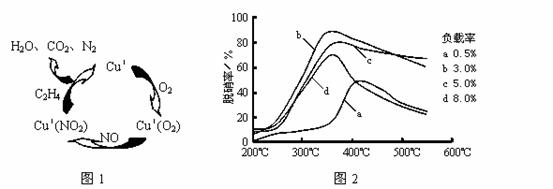
①写出该脱硝原理总反应的化学方程式: 。
②为达到最佳脱硝效果,应采取的条件是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用下图装置可以模拟铁的电化学防护。下列说法不正确的是
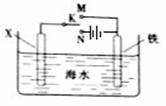
A. 若X为锌棒,开关K置于M处,可减缓铁的腐蚀B. 若X为锌棒,开关K置于M处,铁极发生氧化反应
C. 若X为碳棒,开关K置于N处,可减缓铁的腐蚀D. 若X为碳棒,开关K置于N处,X极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
关于图中各装置的叙述不正确的是
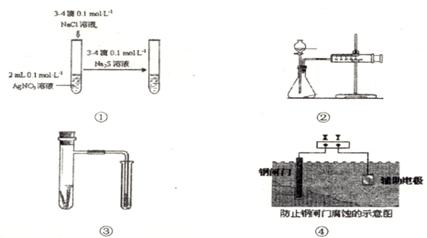
A. 装置①能验证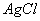 沉淀可转化为溶解度更小的
沉淀可转化为溶解度更小的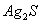 沉淀B. 装置②能测量锌与硫酸的反应速率
沉淀B. 装置②能测量锌与硫酸的反应速率
C. 装置③能验证铁的吸氧腐蚀D. 装置④的X电极是负极,则能验证外接电源的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:
N2 + 3H2  2NH3 ΔH=—92.4 KJ/mol,则N≡N键的键能是 ( )
2NH3 ΔH=—92.4 KJ/mol,则N≡N键的键能是 ( )
A.431 KJ/mol B.946 KJ/mol C.649 KJ/mol D.869 KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要O.1 mol/L NaOH溶液450 mL和0.5mol/l硫酸溶液480 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液需要的是 (填字号),配制上述溶液还需用到的玻璃仪器是 (填仪器名称)。
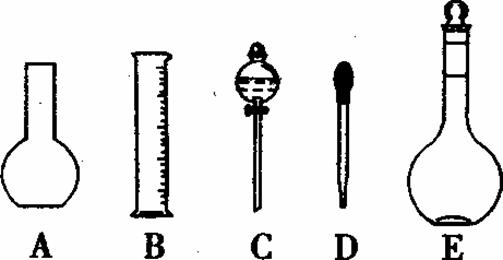
(2)下列操作中,是容量瓶所具备的功能有 。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.配制任意浓度和体积的标准溶液
D.稀释某一浓度的溶液
E.量取一定体积的液体
(3)根据计算用托盘天平称取NaOH的质量为 g。在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度 (填“大于”“等于”或“小于”)O.1 mol/l。若NaOH溶液在转移至容量瓶时,洒落了少许,则需要如何操作: 。(4)根据计算得知,所需质量分数为98%、密度为l.84 g/cm3的浓硫酸的体积为 ml。如果实验室有10 mL,15 mL,20 mL量筒,应选用 mL的量筒最好。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是
(5)下列操作会使配制的NaOH溶液浓度偏低 的是。
A.用滤纸称量NaOH
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.整个配制过程中,容量瓶不振荡
查看答案和解析>>
科目:高中化学 来源: 题型:
将纯锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
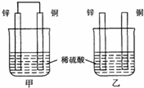 A.两烧杯中溶液的pH均增大
A.两烧杯中溶液的pH均增大
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中铜片表面均无气泡产生
D.甲、乙溶液均变蓝色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com