
【题目】海洋约占地球表面积的71%,对其进行开发利用的部分流程如下图所示。下列说法不正确的是( )

A.可用BaCl2溶液除去粗盐中的SO![]()
B.从苦卤中提取Br2的反应的离子方程式为2Br-+Cl2===2Cl-+Br2
C.试剂1可以选用石灰乳
D.工业上,通常电解氯化镁溶液来冶炼金属镁
科目:高中化学 来源: 题型:
【题目】水热法制备直径为1-100nm的颗粒Y(化合物),反应原理为3Fe2++2![]() +O2+aOH-=Y+
+O2+aOH-=Y+![]() +2H2O,下列说法中不正确的
+2H2O,下列说法中不正确的
A.a=4
B.将Y均匀分散到水中形成的体系具有丁达尔效应
C.Fe2+、![]() 都是还原剂
都是还原剂
D.每有3molFe2+参加反应,反应中转移的电子总数目为5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为ABC三套实验装置。
A、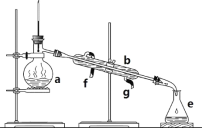 B、
B、 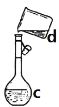 C、
C、 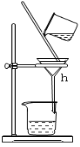
(1)写出下列仪器的名称:b.___, c._____,h.____。
(2)仪器a~e中,使用前必须检查是否漏水的有_____。(填序号)
(3)若利用装置分离酒精和水的混合物,还缺少的仪器是_____,将仪器补充完整后进行实验,冷凝水由____口流出(填f或g)。
(4)现需配制0.1mol/LNaOH溶液450mL,B装置是某同学转移溶液的示意图。
① B 图中的错误是_____。
② 根据计算得知,所需NaOH的质量为_______。
③ 配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)________。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
F.改用胶头滴管加水,使溶液凹面恰好与刻度相切
(5)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。若没有进行A操作_______;容量瓶用蒸馏洗涤后残留有少量的水_________;若定容时俯视刻度线_______。
(6)将(4)所配溶液滴入盛有硫酸铜溶液试管中,可以观察到现象是_____,发生反应的离子方程式为_______,若将得到混合物进行分离,可选用分离方法是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
(1)已知:CO2(g)+H2(g)![]() H2O(g) +CO(g) ΔH1 = + 41.1 kJmol-1
H2O(g) +CO(g) ΔH1 = + 41.1 kJmol-1
CO(g)+2H2(g)![]() CH3OH(g) ΔH2=-90.0 kJmol-1
CH3OH(g) ΔH2=-90.0 kJmol-1
写出CO2催化氢化合成甲醇的热化学方程式:_______。
(2)为提高CH3OH产率,理论上应采用的条件是_______(填字母)。
a.高温高压 b.低温低压 c.高温低压 d.低温高压
(3)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),下图为不同投料比[n(H2)/n(CO2)]时某反应物X平衡转化率变化曲线。
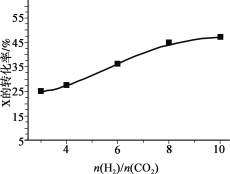
① 反应物X是_______(填“CO2”或“H2”)。
② 判断依据是_______。
(4)250℃、在体积为2.0L的恒容密闭容器中加入6mol H2、2mol CO2和催化剂,10min时反应达到平衡,测得c(CH3OH) = 0.75 mol· L-1。
① 前10min的平均反应速率v(H2)=_______ mol·L-1·min -1。
② 化学平衡常数K = _______。
③ 催化剂和反应条件与反应物转化率和产物的选择性有高度相关。控制相同投料比和相同反应时间,四组实验数据如下:
实验编号 | 温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
A | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
B | 543 | Cu/ZnO纳米片 | 11.9 | 72.7 |
C | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
D | span>553 | Cu/ZnO纳米片 | 12.0 | 70.6 |
根据上表所给数据,用CO2生产甲醇的最优选项为_______(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
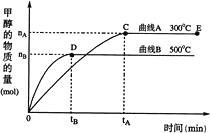
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=_______________,升高温度,K值_______(填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=_____________。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是_______:
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:_______________________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.中国的侯德榜对索尔维制碱法进行了改进,将合成氨工业与纯碱工业联合,发明了侯氏制碱法,又称联合制碱法,生产流程可以表示如图所示(![]() 代表所需物质,
代表所需物质,![]() 代表产品)
代表产品)
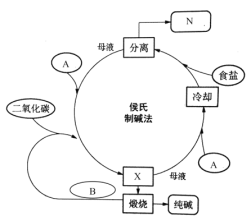
在上述工业流程中:
(1)产品N的化学式__________,所需物质A的名称____________,B的电子式____________。
(2)侯德榜制碱法的原理是_____________________________________(用化学方程式表示)。操作X的名称是_________________________。
II.利用侯德榜原理制备的纯碱中含有少量NaCl等杂质,利用下列装置可用来测定纯碱中的Na2CO3的质量分数。
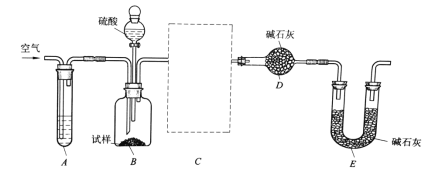
实验步骤如下:
①如图所示,组装好实验仪器,并检查其气密性;
②准确称取盛有碱石灰的干燥管D的质量(设为m1g);
③准确称取一定量的纯碱(设为ng),并将其放进广口瓶B内;
④从分液漏斗中缓缓滴入一定量的稀硫酸,并从前端缓缓地鼓入空气,至B反应器中不再产生气体为止;
⑤准确称取干燥管D的总质量(设为m2g)
根据上述实验,回答下列问题:
(3)该实验进行到操作④时,要缓缓鼓入空气,鼓入空气的作用是__________________________。装置A中的液体应选用___________。
(4)装置B与D之间必须添加一装置C,否则使测定结果偏高。在空白框内画出该装置C,装置中盛放的是__________。
(5)根据此实验,计算出纯碱中Na2CO3的质量分数为_________________(用m1、m2、n表示)。如果缺少装置E,则实验所得纯碱样品的纯度会_________(“偏高”、“偏低”、或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.向CH3COOH中加入适量NaOH溶液:H++OH-=H2O
B.Fe与稀HNO3反应:Fe+2H+=Fe2++H2↑
C.Cl2通入H2O中:Cl2+H2O=2H++Cl-+ClO-
D.AlCl3溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性HSO3->I-,氧化性IO3->I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。
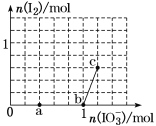
下列说法正确的是( )
A.0~b间的反应可用离子方程式3SO32-+IO3-=3SO42-+I-表示
B.a点时消耗的NaHSO3的物质的量为1.2 mol
C.b点到c点,KIO3与NaHSO3反应生成I2
D.当溶液中I-与I2的物质的量之比为5∶3时,加入的KIO3为1.08 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com