
【题目】下列事实不能用平衡移动原理解释的是
A.配制FeCl3溶液时加入少量的浓盐酸
B.常温下,NaOH溶液中由水电离出的c(H+)<1×10-7mol/L
C.AgCl在水中的溶解度大于在饱和NaCl溶液中的溶解度
D.工业上SO2转化为SO3用五氧化二钒铁触媒作为催化剂
科目:高中化学 来源: 题型:
【题目】原子序数为83的元素位于:① 第五周期;② 第六周期;③ ⅣA族;④ ⅤA族;⑤ ⅡB族,其中正确的组合是( )
A.① ④B.② ③C.② ④D.① ⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种元素的原子序数依次为a、b、c,它们的离子An+、Bm﹣、Cn﹣具有相同的电子层结构,且n<m,则下列关系正确的是( )
A.a>b>c
B.b>a>c
C.a=b+m+n
D.a=c﹣n﹣m
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Fe(OH)3胶体微粒能吸附Fe3+离子。在约50mL的沸水中,滴入8—10滴(20滴约为1mL)饱和FeCl3溶液至其为红褐色后,将它们装入半透膜袋中,并浸没在盛有蒸馏水的烧杯中。隔一段时间后,烧杯里的水中含有的离子最多的是 ( )
A. H+、OH- B. H+、Cl- C. Fe3+、Cl- D. Fe3+、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与胶体性质无关的是( )
A.在豆浆里加入盐卤做豆腐
B.河流入海处易形成沙洲
C.一束平行光线照射蛋白质溶液时,从侧面可以看到光亮的通路
D.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用。某型甲醇燃料电池的总反应式2CH40+302=2C02↑+4H20,下图是该燃料电池的示意图。
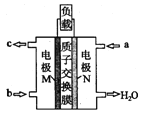
下列说法错误的是
A.燃料电池将化学能转化为电能
B.a是甲醇,b是氧气
C.质子从M电极区穿过交换膜移向N电极区
D.负极反应:CH40-6e-+H20=C02↑+6H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.开发新能源,新材料是实现社会可持续发展的需要。下图是LiBH4/MgH2体系放氢的焓变示意图,则Mg(s)+2B(s)==MgB2(s)的ΔH=_________kJ·mol-1。
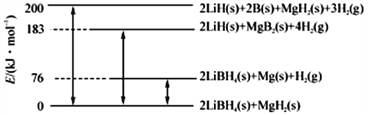
Ⅱ.在1.0L恒容密闭容器中放入0.10mol A(g),在一定温度时进行如下反应:A(g)==2B(g)+C(g)+D(S) ΔH=+85.1kJ·mol-1。
容器内气体总压强P与起始压强P0的比值随反应时间变化数据见下表:
时间t/min | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
P/P0 | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
回答下列问题:
(1)下列能提高A的转化率的是______________。
A.升高温度 B.向体系中通入气体A
C. 减少D的物质的量 D.向体系中通入稀有气体
(2)下列说法能表明该反应达到化学平衡状态的是_______________。
A.A、B、C的物质的量之比为1∶2∶1 B.单位时间内生成2n mol B,同时生成n mol C
C.容器中气体的密度不变 D.容器中气体的平均摩尔质量不变
(3)达到平衡状态时A的转化率是________(结果保留两位有效数字)。
(4)相同条件下,若该反应从逆向开始,建立与上述相同的化学平衡,则D的取值范围为n(D)_______ mol。
(5)相同条件下,若将容器改为恒压容器,进行上述反应,某时刻,A的转化率为75%,则此时B的物质的量浓度为______________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两容器,甲容器容积固定,乙容器容积可变。一定温度下,在甲中加入2 mol N2、3 mol H2,反应N2(g)+3H2(g)![]() 2NH3(g)达到平衡时生成NH3的物质的量为m mol。
2NH3(g)达到平衡时生成NH3的物质的量为m mol。
(1)相同温度下,在乙中加入4 mol N2、6 mol H2,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成NH3的物质的量为________mol(从下列各项中选择,只填序号,下同);若乙的容积与甲的容积始终相等,乙中反应达到平衡时,生成NH3的物质的量为________mol。
A.小于m B.等于m C.在m~2m之间 D.等于2m E.大于2m
(2)相同温度下,保持乙的容积为甲的一半,并加入1 mol NH3,要使乙中反应达到平衡时,各物质的体积分数与上述甲容器中达到平衡时相同,则起始应加入______mol N2和________mol H2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com