
【题目】下列有关电解质溶液中微粒的物质的量浓度关系正确的是
A.向![]() 溶液中加入等体积
溶液中加入等体积![]() 溶液:
溶液:![]()
B.物质的量浓度都为![]() 的
的![]() 与
与![]() 溶液等体积混合后,
溶液等体积混合后,![]()
C.已知常温下,![]() 的电离常数
的电离常数![]() ,
,![]() .
.![]() 溶液:
溶液:![]()
D.![]() 溶液与
溶液与![]() 溶液混合:
溶液混合:![]()
【答案】D
【解析】
A.向0.2mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液,二者反应生成碳酸钠和水,溶液中溶质为0.05mol·L-1的NaHCO3和Na2CO3;
B.物质的量浓度都为![]() 的
的![]() 与
与![]() 溶液等体积混合后,溶液变成CH3COONa溶液,根据物料守恒分析;
溶液等体积混合后,溶液变成CH3COONa溶液,根据物料守恒分析;
C.![]() 溶液要先判断水解和电离的大小,确定溶液的酸碱性;
溶液要先判断水解和电离的大小,确定溶液的酸碱性;
D.![]() 溶液与
溶液与![]() 溶液混合,相当于等物质的量浓度的NH3·H2O和NaCl的混合溶液,由此分析。
溶液混合,相当于等物质的量浓度的NH3·H2O和NaCl的混合溶液,由此分析。
A.向0.2mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液,二者反应生成碳酸钠和水,溶液中溶质为0.05mol·L-1的NaHCO3和Na2CO3,NaHCO3和Na2CO3水解导致溶液呈碱性,且碳酸钠水解程度大于碳酸氢钠,所以c(HCO![]() )>c(CO
)>c(CO![]() )>c(OH-)>c(H+),故A错误;
)>c(OH-)>c(H+),故A错误;
B.物质的量浓度都为![]() 的
的![]() 与
与![]() 溶液等体积混合后,溶液变成
溶液等体积混合后,溶液变成![]() 的CH3COONa溶液,根据物料守恒,
的CH3COONa溶液,根据物料守恒,![]() ,故B错误;
,故B错误;
C.NaHC2O4溶液中水解:HC2O![]() +H2O
+H2O![]() H2C2O4+OH-,其水解平衡常数的表达式为Kh2=
H2C2O4+OH-,其水解平衡常数的表达式为Kh2=![]() ,然后变形,即上下同乘以c(H+),得到Kh2=
,然后变形,即上下同乘以c(H+),得到Kh2=![]() =1.85×10-13<
=1.85×10-13<![]() ,说明HC2O4-的电离程度大于其水解,溶液显酸性,
,说明HC2O4-的电离程度大于其水解,溶液显酸性,![]() 溶液:
溶液:![]() ,故C错误;
,故C错误;
D.![]() 溶液与
溶液与![]() 溶液混合,相当于等物质的量浓度的NH3·H2O和NaCl的混合溶液,氯化钠是强电解质,不水解,显中性,而一水合氨发生部分电离,溶液呈碱性:
溶液混合,相当于等物质的量浓度的NH3·H2O和NaCl的混合溶液,氯化钠是强电解质,不水解,显中性,而一水合氨发生部分电离,溶液呈碱性:![]() ,故D正确;
,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】已知NA为阿伏加德罗常数的值,下列叙述正确的是
A.1L0.1mol/LNH4Cl溶液中,![]() 的数量为0.1NA
的数量为0.1NA
B.0.1mol的14C中,含有0.6NA个中子
C.标准状况下,2.24LN2和O2的混合气体中原子数为0.2NA
D.16g甲烷和1mol白磷中含有的化学键数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的顺序为SO2>I->Fe2+>H2O2>Cl-,则下列反应不可能发生的是
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气净化原理为2NO(g)+2CO(g)N2(g)+2CO2(g)ΔH=-746.5kJ·mol-1,如图为在不同初始浓度的CO和不同催化剂Ⅰ、Ⅱ作用下(其他条件相同),体积为2L的密闭容器中n(N2)随反应时间的变化曲线,下列说法正确的是( )
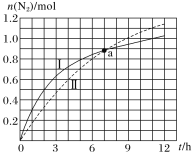
A.a点时,催化剂Ⅰ、Ⅱ作用下CO的转化率相等
B.0~6h内,催化剂Ⅰ的催化效果比催化剂Ⅱ的好
C.0~5h内,催化剂Ⅰ作用下CO的反应速率为0.32mol·L-1·h-1
D.0~12h内,催化剂Ⅱ作用下反应放出的热量比催化剂Ⅰ的多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应的实验,能达到实验目的的是
A.  所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验
所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验
B.  所示装置验证二氧化硫的漂白性
所示装置验证二氧化硫的漂白性
C.  所示装置分离四氯化碳和苯的混合物
所示装置分离四氯化碳和苯的混合物
D.  所示装置检验氯化铵受热分解生成的两种气体
所示装置检验氯化铵受热分解生成的两种气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物![]() 同时满足下列条件:①含苯环且不含甲基;②苯环上一氯取代物只2种;③
同时满足下列条件:①含苯环且不含甲基;②苯环上一氯取代物只2种;③![]() 与足量的
与足量的![]() 反应生成
反应生成![]() ;④遇
;④遇![]() 溶液不显色.A如图所示转化关系:
溶液不显色.A如图所示转化关系:
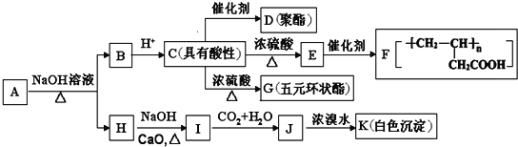
已知:![]()
回答下列问题:
(1)E中官能团名称_____,H的分子式为_______.
(2)由C生成G的反应类型是________.
(3)A的结构简式为____,G的结构简式为_________.
(4)①写出CD反应的化学方程式_________;
②写出I→J反应的离子方程式_____________.
(5)C的同分异构体中能同时满足下列条件:a.能发生银镜反应,b.能发生皂化反应;c.能与![]() 反应产生
反应产生![]() ,共有_____种(不含立体异构).其中核磁共振氡谱显示为3组峰,且峰面积比为6:1:1的是_________(写结构简式).
,共有_____种(不含立体异构).其中核磁共振氡谱显示为3组峰,且峰面积比为6:1:1的是_________(写结构简式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列说法错误的是 ( )
A.疫苗一般应冷藏存放,以避免蛋白质变性
B.医用口罩无纺布的原材料成分之一是聚丙烯,其结构简式为![]()
C.使用医用酒精杀菌消毒的过程中只发生了物理变化
D.医用防护服的核心材料是微孔聚四氟乙烯薄膜,其单体四氟乙烯属于卤代烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.除去FeSO4 溶液中的 Fe3+, 可向溶液中加入铜粉, 通过反应 Cu + 2Fe3+ = Cu2+ + 2Fe2+除去 Fe3+
B.常温下,pH为5的 NH4Cl 溶液和pH为5的稀盐酸中,水的电离程度相同
C.由于存在水的电离,0.1 molL-1 的 H2C2O4溶液中, c(H+)/c(C2O![]() )略大于2
)略大于2
D.向氨水中滴加等浓度的盐酸溶液,滴加过程中,c(NH![]() )先增大后减小
)先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林的有效成分是乙酰水杨酸(![]() )。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
)。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
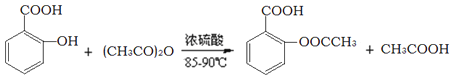
操作流程如下:

已知:水杨酸和乙酰水杨酸均微溶于水,但其钠盐易溶于水,醋酸酐遇水分解生成醋酸。
回答下列问题:
(1)合成过程中最合适的加热方法是______________。
(2)提纯粗产品流程如下,加热回流装置如图:
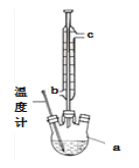
①沸石的作用是_______________;
②冷凝水的流出方向是____________(填“b”或“c”);
③使用温度计的目的是____________。
(3)检验最终产品中是否含有水杨酸的化学方法是_________________。
(4)阿司匹林药片中乙酰水杨酸含量的测定步骤(假定只含乙酰水杨酸和辅料,辅料不参与反应):
Ⅰ.称取阿司匹林样品m g;Ⅱ.将样品研碎,溶于V1 mL a mol·L-1NaOH(过量)并加热,除去辅料等不溶物,将所得溶液移入锥形瓶;Ⅲ.向锥形瓶中滴加几滴酚酞,用浓度为b mol·L-1的标准盐酸到滴定剩余的NaOH,消耗盐酸的体积为V2mL。
① 写出乙酰水杨酸与过量NaOH溶液加热发生反应的化学方程式______________。
② 阿司匹林药片中乙酰水杨酸质量分数的表达式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com