
【题目】在100℃时,将0.01mol的四氧化二氮气体充入0.1L的密闭容器中,发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
时间/s 浓度/(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4) | 0.100 | 0.070 | 0.050 | c3 | a | b |
c(NO2) | 0 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
请填空:
(1)该反应的化学方程式为____________。达到平衡时N2O4的转化率为____________,表中c2____________c3;a____________b(填“>”“<”或“=”)。
(2)在0~20s内,N2O4的平均反应速率为____________。
【答案】![]() 60% > = 0.0015
60% > = 0.0015![]()
【解析】
从分析表格数据找出反应方程式为N2O4![]() 2NO2,按定义 进行转化率的计算,通过计算,比较c2 和c3的相对大小,按反应速率的定义计算的N2O4速率;
2NO2,按定义 进行转化率的计算,通过计算,比较c2 和c3的相对大小,按反应速率的定义计算的N2O4速率;
(1)通过表格知,N2O4是反应物,NO2是生成物,则反应方程式为N2O4![]() 2NO2,达到化学平衡时NO2的浓度是0.120mol/L,则达到平衡过程中消耗N2O4的物质的量浓度
2NO2,达到化学平衡时NO2的浓度是0.120mol/L,则达到平衡过程中消耗N2O4的物质的量浓度![]() ,则转化率为
,则转化率为![]() ,达到平衡时N2O4物质的量浓度c3=
,达到平衡时N2O4物质的量浓度c3=![]() ,故40s还没达到化学平衡,40s时生成NO2的物质的量浓度c2=
,故40s还没达到化学平衡,40s时生成NO2的物质的量浓度c2=![]() ,即C2>C3,a=b;
,即C2>C3,a=b;
答案为:N2O42NO2;60%;>;=;
(2)20s时消耗N2O4的物质的量浓度![]() , 0~20s平均反应速率
, 0~20s平均反应速率![]() ;
;
答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图.下列说法正确的是 ( )
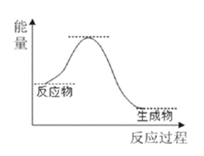

A.NH3催化还原NO为吸热反应
B.过程Ⅰ中NH3断裂非极性键
C.过程Ⅱ中NO为氧化剂,Fe2+为还原剂
D.脱硝的总反应为: 4NH3(g)+4NO(g)+ O2(g) ![]() 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写正确的是( )
A. 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+===Fe2+ + 2Fe3+ + 4H2O
B. Na2O2 加入H218O 中:2Na2O2 + 2H2l8O ===4Na+ + 4OH-+ 18O2↑
C. 水玻璃中通入过量二氧化碳:Na2SiO3 +CO2 + H2O===2Na+ +CO32- + H2SiO3↓
D. 成分为盐酸的洁厕灵与“84”消毒液混合使用易中毒:C1—+ C1O—+ 2H+=== Cl2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应2AB(g)![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 单位时间内生成nmolA2,同时消耗2n molAB
B. 容器内,3种气体AB、A2、B2共存
C. AB的消耗速率等于A2的消耗速率
D. 容器中各组分的体积分数不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3A(g)+B(g)=2C(g)+2D(g)在四中不同条件下用不同物质表示的化学反应速率如下,其中最快的是
A.v(A)=0.3mol/(L·s)B.v(B)=12mol/(L·min)
C.v(C)=0.15mol/(L·s)D.v(D)=15mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下物质间的每一步转化都能通过一步反应实现的是( )
①Fe → FeCl2 → Fe(OH)2 → Fe(OH)3
②Si → SiO2 → H2SiO3 → Na2SiO3
③Al → Al2O3 → Al(OH) 3 → AlCl3
④NH3 →NO2 → HNO3 → NH4NO3
⑤Na → Na2O → Na2CO3 → NaHCO3 → NaOH
A.②③⑤B.①⑤C.①④⑤D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氨的叙述中不正确的是( )
A. 氨分子中氮元素的化合价只能升高,氨具有还原性
B. 氨的催化氧化反应的化学方程式是4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
C. 氨的催化氧化反应中若氧气过量则有红棕色气体生成
D. 氨的催化氧化属于人工氮的固定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用核磁共振技术测定有机物分子的三维结构的研究曾获得诺贝尔化学奖。在有机物分子中,不同位置的氢原子的核磁共振谱中给出的峰值(信号)也不同。根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
(1)下列分子中,其核磁共振氢谱中只有一种峰(信号)的物质是_______(多选)。
A.CH3-CH3 B.CH3COOH C.CH3COOCH3 D.CH3COCH3
(2)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱如下图所示,则A的结构简式为_______,请预测B的核磁共振氢谱上有______个峰(信号)。
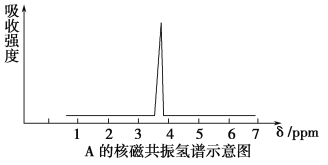
(3)用核磁共振氢谱的方法来研究C2H6O的结构,请简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2012年2月,江苏镇江自来水出现异味,引发镇江及位于其下游的南通等地区发生居民抢购瓶装饮用水的现象。经初步调查,韩国籍船舶“格洛里亚”号货轮水下排放管道排出的苯酚是引起自来水异味的主要原因。请完成以下填空:
(1)苯酚与水混合,溶液变浑浊,向该浑浊液中滴加NaOH溶液,可观察到的现象是____,向上述反应液中继续通入过量CO2,又可观察到的现象是____,则通入CO2时的反应为_____,说明苯酚具有_______性。
(2)A和B两种物质的分子式都是C7H8O,它们都能跟金属钠反应放出氢气。B能使适量溴水褪色,并产生白色沉淀,A不能。B苯环上的一溴代物有两种。
①写出A和B的结构简式:A________,B_______________。
②写出B与NaOH溶液反应的化学方程式:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com