
【题目】可逆反应:3A(g) ![]() 3B+C△H > 0,随着温度升高,气体平均分子质量有变小趋势,则下列判断正确的是( )
3B+C△H > 0,随着温度升高,气体平均分子质量有变小趋势,则下列判断正确的是( )
A.若C为固体,则B一定是气体B.B和C一定都是固体
C.B和C可能都是固体D.B和C不可能都是气体
【答案】A
【解析】
反应是吸热反应,升温平衡正向进行,气体平均摩尔质量=![]() ,依据概念中的气体质量、气体物质的量分析判断。
,依据概念中的气体质量、气体物质的量分析判断。
3A(g) ![]() 3B+C△H>0,该正反应吸热,温度升高,平衡右移,平均摩尔质量变小,依据反应的系数关系,气体平衡体系的质量守恒,平均摩尔质量的变化,由反应前后气体物质的量变化、混合气体的质量变化决定;
3B+C△H>0,该正反应吸热,温度升高,平衡右移,平均摩尔质量变小,依据反应的系数关系,气体平衡体系的质量守恒,平均摩尔质量的变化,由反应前后气体物质的量变化、混合气体的质量变化决定;
A. C为固体,B一定为气体,反应前后气体物质的量不变,气体质量减小,平均摩尔质量减小,故A正确;
B. B和C一定是固体时,只有A一种气体,平均摩尔质量不变,故B错误;
C. B和C可能都是固体时,只有A一种气体,平均摩尔质量不变,故C错误;
D.若B和C都是气体,气体总质量不变,升温平衡正向进行,气体物质的量增大,气体平均摩尔质量减小,故D错误;
答案选A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
Ⅰ(pH=2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
Ⅱ(pH=4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
Ⅳ(pH=4,含Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
下列说法不正确的是
A. 在0~20min内,I中M的分解速率为0.015 mol·L-1·min-1
p>B. 水样酸性越强,M的分解速率越快C. 在0~25min内,III中M的分解百分率比II大
D. 由于Cu2+存在,IV中M的分解速率比I快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g)![]() xC(g)+D(s),向甲中通入6mol A和2mol B,向乙中通入1.5mol A、0.5mol B、3mol C和2mol D,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为20%,下列叙述中不正确的是( )
xC(g)+D(s),向甲中通入6mol A和2mol B,向乙中通入1.5mol A、0.5mol B、3mol C和2mol D,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为20%,下列叙述中不正确的是( )
A.若平衡时,甲、乙两容器中A的物质的量不相等,则x=4
B.平衡时,甲、乙两容器中A、B的物质的量之比相等
C.平衡时甲中A的体积分数为40%
D.若平衡时两容器中的压强不相等,则两容器中压强之比为8:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁[Mgx(CO3)y(OH)z·wH2O]的主要流程如图:

(1)“溶解”时,加快溶解速率的措施有_______________(写一条)。
(2)“滤液”中的溶质主要有______________(写化学式)。
(3)已知高温煅烧碱式碳酸镁可得到MgO。请写出煅烧碱式碳酸镁发生的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应N2+3H2![]() 2NH3达到化学平衡状态,下列说法一定正确的是( )
2NH3达到化学平衡状态,下列说法一定正确的是( )
A.每1 mol N≡N断裂的同时有2 mol N—H生成
B.N2、H2、NH3的浓度之比为1∶3∶2
C.N2减少的速率和NH3减少的速率之比为1∶2
D.气体体积为初始体积的0.7倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化剂H2O2在反应时不产生污染物被称为“绿色氧化剂”,因而受到人们越来越多的关注。
Ⅰ.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。

(1)实验①和②的目的是___________。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是__________(填一种方法即可)。
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图1所示。分析该图能够得出的实验结论是_______________。



Ⅱ.资料显示,某些金属离子或金属氧化物对H2O2的分解起催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如图2所示的实验装置进行实验。
(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量_________或________来比较。
(2)0.1 g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示。请解释化学反应速率变化的原因:_______。请计算H2O2的初始物质的量浓度为__________(保留两位有效数字)。为探究MnO2在此实验中对H2O2的分解起催化作用,需补做下列实验(无需写出具体操作):a._______;b._______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知M(g)+N(g) ![]() P(g)+Q(g)反应的平衡常数和温度的关系如下:
P(g)+Q(g)反应的平衡常数和温度的关系如下:
|温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答:
(1)该反应的平衡常数表达式K=_____________ ,△H_____0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的M和0.80mol的N,若反应6s内M的平均反应速率v(M)=0.003 mol·L-1·s-1。,则6s时c(M)=______ mol·L-1, P的物质的量为_______mol;若反应经一段时间后,达到平衡时N的转化率为______。
(3)判断该反应是否达到平衡的依据为_______(填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c. c(M)不随时问改变 d.单位时间里生成P和Q的物质的量相等
(4)1200℃时反应P(g)+Q(g) ![]() M(g)+N(g)的平衡常数的值为______________。
M(g)+N(g)的平衡常数的值为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g)![]() CO2(g)+N2(g),平衡时c(NO)与温度T的关系如下图所示,则下列说法不正确的是
CO2(g)+N2(g),平衡时c(NO)与温度T的关系如下图所示,则下列说法不正确的是
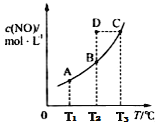
A. 该反应正反应的△H<0
B. 若状态A、B的逆反应速率分别为v逆(A)、v逆(B),则v逆(A)>v逆(B)
C. 在T2时,若反应体系处于状态D,则此时v正>v逆
D. 若状态B、C、D的压强分别为PB、PC、PD,则 PC>PD=PB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室为探究铁与浓硫酸![]() 足量
足量![]() 的反应,并验证
的反应,并验证![]() 的性质,设计如图所示装置进行实验,下列说法不正确的是()
的性质,设计如图所示装置进行实验,下列说法不正确的是()

A.装置B中酸性![]() 溶液逐渐褪色,体现了二氧化硫的还原性
溶液逐渐褪色,体现了二氧化硫的还原性
B.实验结束后可向装置A的溶液中滴加KSCN溶液以检验生成的![]()
C.装置D中品红溶液褪色可以验证![]() 的漂白性
的漂白性
D.实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com