
����Ŀ�����ݻ�һ�����ܱ������У�����һ������һ������������̼������ѧ��Ӧ��C��s��+2NO��g��![]() CO2��g��+N2��g����ƽ��ʱc��NO�����¶�T�Ĺ�ϵ����ͼ��ʾ��������˵������ȷ����
CO2��g��+N2��g����ƽ��ʱc��NO�����¶�T�Ĺ�ϵ����ͼ��ʾ��������˵������ȷ����
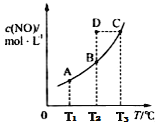
A. �÷�Ӧ����Ӧ����H��0
B. ��״̬A��B���淴Ӧ���ʷֱ�Ϊv����A����v����B������v����A����v����B��
C. ��T2ʱ������Ӧ��ϵ����״̬D�����ʱv����v��
D. ��״̬B��C��D��ѹǿ�ֱ�ΪPB��PC��PD���� PC��PD=PB
���𰸡�B
��������
A����ͼ��֪���¶�Խ��ƽ��ʱc��NO��Խ�������¶�ƽ�����ƣ�
B����ͼ��֪��״̬A���¶�С��״̬B���¶ȣ������¶ȣ���ѧ��Ӧ���ʼӿ죻
C����ͼ��֪��T2ʱ��Ӧ���е�״̬D��c��CO������ƽ��Ũ�ȣ��ʷ�Ӧ���淴Ӧ���У�
D���ﵽƽ��״̬ʱ��ѹǿ���¶ȳ���������ϵ��
A���ͼ��֪���¶�Խ��ƽ��ʱc��NO��Խ�������¶�ƽ�����ƣ���������ӦΪ���ȷ�Ӧ������H��0����A��ȷ��
B���ͼ��֪��״̬A���¶�С��״̬B���¶ȣ������¶ȣ���ѧ��Ӧ���ʼӿ죬��v����B����v����A������B����
C�T2ʱ��Ӧ���е�״̬D��c��NO������ƽ��Ũ�ȣ��ʷ�Ӧ������Ӧ���У���һ����v����v������C��ȷ��
D��ﵽƽ��״̬ʱ��ѹǿ���¶ȳ���������ϵ��ѹǿ��СΪPC��PD=PB����D��ȷ��
��ѡB��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA���������ӵ�������ֵ��������Ȼ�ѧ����ʽC2H2��g��+![]() O2(g) ��2CO2(g)+H2O(l) ��H=��1300 kJ��mol��1��˵���У���ȷ����( )
O2(g) ��2CO2(g)+H2O(l) ��H=��1300 kJ��mol��1��˵���У���ȷ����( )
A����10NA������ת��ʱ���÷�Ӧ����1300 kJ������
B����1NA��ˮ����������ΪҺ��ʱ������1300 kJ������
C����2NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ������
D����8NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��3A(g) ![]() 3B+C��H > 0,�����¶����ߣ�����ƽ�����������б�С���ƣ��������ж���ȷ����( )
3B+C��H > 0,�����¶����ߣ�����ƽ�����������б�С���ƣ��������ж���ȷ����( )
A.��CΪ���壬��Bһ��������B.B��Cһ�����ǹ���
C.B��C���ܶ��ǹ���D.B��C�����ܶ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ɷ������·�Ӧ��P4+5O2=P4O10����֪�������л�ѧ����Ҫ���յ������ֱ�Ϊ��P-P a kJ/mol��P-O b kJ/mol��P=O c kJ/mol��O=O d kJ/mol�������й����ݺ���ͼ��ʾ�ķ��ӽṹ����÷�Ӧ��H��������ȷ����( )

A.(6a+5d-4c-12b)kJmol-1B.(4c+12b-6a-5d) kJmol-1
C.(4c+12b-4a-5d) kJmol-1D.(4a+Sd-4c-12b) kJmol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ݻ�ѧ֪ʶ�ش��������⣺
(1)ʵ����0.16g CH4��ȫȼ������224mLCO2(��״��)��0.36gҺ̬ˮ�����ų�8.903kJ����������CH4��ȼ����Ϊ________kJmol-1��
(2)̼�����Ƚ��ƶ������̷��������У�
i��MnCO3(s)![]() MnO(s)+CO2(g) H1=+a kJmol-1
MnO(s)+CO2(g) H1=+a kJmol-1
ii��2MnO (s)+ O2(g)![]() 2MnO2(s) H2=+b kJmol-1
2MnO2(s) H2=+b kJmol-1
��д������MnCO3��ȡMnO2���Ȼ�ѧ����ʽ��______________________________________��
(3)������ijͬѧ̽�����淴Ӧ2NO2(g)![]() N2O4(g) H=-56.9 kJmol-1�IJ���ʵ�鱨�棬�ݴ˻ش����⡣
N2O4(g) H=-56.9 kJmol-1�IJ���ʵ�鱨�棬�ݴ˻ش����⡣

���ձ���NO2��ĺ���ɫ��dz��˵��ƽ��2NO2(g)![]() N2O4(g)��________(�����Ӧ�����淴Ӧ��)�����ƶ�������NH4NO3��������ˮ��________(����ȡ������ȡ�)���̡�
N2O4(g)��________(�����Ӧ�����淴Ӧ��)�����ƶ�������NH4NO3��������ˮ��________(����ȡ������ȡ�)���̡�
(4)25��Cʱ���������ʵĵ���ƽ�ⳣ�������ʾ��
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | 1.7��10-5 | K1=4.3��10-7 K2=5.6��10-11 | 3.0��10-8 |
�������ж�CH3COOH��H2CO3��HClO��������ǿ������˳����________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮú����ԭ������![]() ������һ����ӦΪ
������һ����ӦΪ![]()
![]() ����һ��ѹǿ�·����÷�Ӧ��ƽ��ʱ
����һ��ѹǿ�·����÷�Ӧ��ƽ��ʱ![]() ���������ת����
���������ת����![]() ��ԭ����Ͷ�ϱ�
��ԭ����Ͷ�ϱ�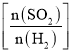 ���¶�
���¶�![]() �Ĺ�ϵ��ͼ��ʾ������˵������ȷ����
�Ĺ�ϵ��ͼ��ʾ������˵������ȷ����
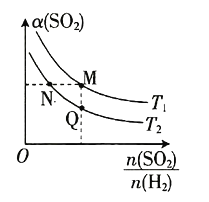
A.����Ӧ�Ļ��![]() B.
B.![]() ��
��![]()
C.�淴Ӧ���ʣ�![]() D.����ѹǿ��
D.����ѹǿ��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����ijһԪ��HA��NaOH��Һ��������(����仯���Բ���)����÷�Ӧ����Һ��pH���±��������жϲ���ȷ���ǣ� ��
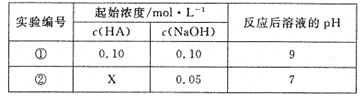
A.X>0.05
B.��ʵ����������Һ��ˮϡ�ͺ�c(OH�� )/c(A��)���
C.ʵ����������Һc(A-)+c(HA)=0.10mol��L-1
D.ʵ����������Һ�� c(Na+)+c(OH-)= c(A-)+c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����Ȼ�ѧ����ʽ�У���H1>��H2���ǣ� ��
��C(s)��O2(g)=CO2(g) ��H1 C(s)��![]() O2(g)=CO(g) ��H2
O2(g)=CO(g) ��H2
��S(s)��O2(g)=SO2(g) ��H1 S(g)��O2(g)=SO2(g) ��H2
��H2(g)��![]() O2(g)=H2O(l) ��H1 2H2(g)��O2(g)=2H2O(l) ��H2
O2(g)=H2O(l) ��H1 2H2(g)��O2(g)=2H2O(l) ��H2
��CaCO3(s)=CaO(s)��CO2(g) ��H1 CaO(s)��H2O(l)=Ca(OH)2(s) ��H2
A.�٢ڢ�B.�٢ۢ�C.�ڢۢ�D.�٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ش��������⣺
(1)25��ʱ��pH=5��CH3COOH��Һ�У���������NaOH���壬����Һ��![]() _______(����������������С������������)��
_______(����������������������������)��
(2)25���£���ijNa2CO3��Һ�м���ϡ���ᣬ���к�̼Ԫ�صĸ��������ʵ�����������������ҺpH�仯�IJ��������ͼ��ʾ��
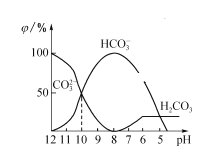
����ͬһ��Һ��,H2CO3��HCO3-��CO32-______�����������������������������档
����pH =7ʱ,��Һ�к�̼Ԫ�ص�����ҪΪ________����Һ�и������ӵ����ʵ���Ũ�ȴ�С��ϵΪ___________________________��
����Ӧ��CO32-+H2O![]() HCO3-+OH-��ƽ�ⳣ��KhֵΪ_________��
HCO3-+OH-��ƽ�ⳣ��KhֵΪ_________��
(3)������H2S��ԭ��Ϊ:H2S+Fe2(SO4)3=S��+2FeSO4+H2SO4��4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O��
2Fe2(SO4)3+2H2O��
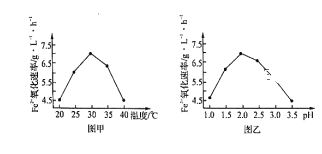
����˾�����ʱ,FeSO4����������������ʱ��5��105�����þ���������___________��
����ͼ��ͼ���ж�ʹ����˾����������Ϊ____________������������£��÷�Ӧ�ļ���
��ʽΪ_________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com