
A、B、C、D、E五种短周期元素的原子序数依次增大,A和D,C和E分别同主族,E的原子序数为C的两倍,B的最外层电子数为A的最外层电子数的4倍。下列叙述正确的是
A.A、B、C三种元素形成的化合物一定是非电解质
B.A与C只能形成化学式为A2C的化合物
C.第三周期中,D的原子半径最大
D.E的氧化物对应的水化物一定具有强氧化性
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源:2014-2015学年北京市顺义区高三第一次统一练习化学试卷(解析版) 题型:选择题
下列叙述不正确的是
A.植物油的不饱和程度高于动物油,植物油更易氧化变质
B.除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液
C.过氧化钠中含有离子键和非极性共价键,阴离子与阳离子的物质的量之比为1:1
D.向某溶液中滴入稀盐酸产生使澄清石灰水变浑浊的气体,该溶液不一定含有CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三4月质量检查理综化学试卷(解析版) 题型:实验题
(16分)某化学兴趣小组进行有关电解食盐水的探究实验,电解装置如右图所示。
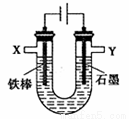
实验一:电解饱和食盐水。
(1)简述配制饱和食盐水的操作:
(2)电解饱和食盐水的离子方程式为
实验二:电解不饱和食盐水及产物分析。
相同条件下,电解1 mol·L一1NaCl溶液并收集两极产生的气体。在X处收集到V1mL气体,同时,在Y处收集到V2mL气体,停止电解。结果发现V2<V1,且与电解饱和食盐水相比,Y处收集到的气体颜色明显较浅。经讨论分析,导致上述现象的原因有:
i.有部分C12溶解于NaCl溶液中;ii.有02生成。
(3)设计实验证明有部分C12溶解于NaCl溶液中。实验方案为 。
(4)证明有O2生成并测定O2的体积。
按如图所示装置进行实验。通过注射器缓缓地将在Y处收集到的V2mL气体全部推入装置A(盛有足量试剂)中,最终,量气管中收集到V3mL气体(设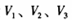 均在相同条件下测得)。
均在相同条件下测得)。
①装置A的作用是 。
②本实验中,观察到 的现象,说明石墨电极上有02生成。
③实验中是否需要预先除净装置中的空气? (填“是”或“否”)。
(5)实验二中,在石墨电极上生成Cl2的总体积为 mL(用代数式表示)。
实验反思:
(6)由以上实验推知,欲通过电解食盐水持续地获得较纯净的氯气,电解时应控制的条件:
① ;② 。要进一步证明该推论,还需进行电解不同浓度食盐水的平行实验。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省西安市高三下学期二模考试理综化学试卷(解析版) 题型:填空题
[化学——选修3:物质结构与性质](15分)第ⅢA、ⅤA族元素组成的化合物AlN、AlP、AlAs等是人工合成的半导体材料,它们的晶体结构与单晶硅相似,与NaCl的晶体类型不同。
(1)核电荷数比As小4的原子基态的电子排布式为_________________________。
(2)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有______种。
(3)NCl3中心原子杂化方式为________________,NCl3的空间构型为__________。
(4)在AlN晶体中,每个Al原子与________个N原子相连,AlN属于________晶体。
(5)设NaCl的摩尔质量为Mr g·mol-1,食盐晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA。食盐晶体中两个距离最近的钠离子中心间的距离为________cm。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省西安市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法正确的是
A.7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA
B.12.5mL 16mol·L-1浓硫酸与足量铜反应,转移电子数为0.2NA
C.5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA
D.标准状况下,22.4 L氧气作氧化剂时转移电子数为4NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高三3月教学质量监测理综化学试卷(解析版) 题型:实验题
(15分)2Na2CO3·3H2O2是一种新型的氧系漂白剂。某实验兴趣小组进行了如下实验。
Ⅰ.实验制备
实验原理:2Na2CO3+3H2O2=2Na2CO3·3H2O2
实验步骤:取3.5 g Na2CO3溶于10 mL H2O,加入0.1 g稳定剂,用磁力搅拌器搅拌完全溶解后,将6.0 mL 30%H2O2在15 min内缓慢加入到三颈烧瓶中,实验装置如图。
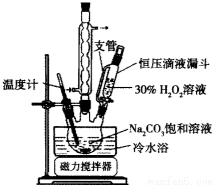
反应1小时后,加入1g氯化钠后,静置结晶,然后抽滤,干燥一周后,称重。
(1)装置中球形冷凝管的作用是______________。
(2)使用冷水浴的作用是______________________________________________。
(3)加入适量NaCl固体的原因是_______________________________________。
(4)2Na2CO3·3H2O2极易分解,其反应方程式可表示为_________________________________。
Ⅱ.活性氧含量测定
准确称取试样0.2000 g,置于250 mL锥形瓶中,加100 mL浓度为6%的硫酸溶液,用0.0200 mol/L高锰酸钾标准溶液滴定,记录高锰酸钾标准溶液消耗的体积为
32.70 mL。
活性氧含量计算公式:Q%=(40cV/m)×100%[c KMnO4标准溶液浓度(mol/L);V
KMnO4标准溶液浓度(mol/L);V 消耗的KMnO4标准溶液体积(L);m
消耗的KMnO4标准溶液体积(L);m 试样质量(g)]
试样质量(g)]
(5)滴定终点的判断依据为______________________________________________。
(6)滴定过程中涉及的化学方程式_______________________________________。
(7)活性氧含量为__________________________。
Ⅲ.产品纯度的测定
(8)为了测定产品中2Na2CO3·3H2O2的质量分数,设计了几种方案,涉及不同的反应原理。
方案一 将试样与MnO2混合均匀,向混合物中滴加水,测生成气体的体积,进而进行计算。
方案二 _________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省新校高三4月模拟化学试卷(解析版) 题型:选择题
短周期中的A、B、C、D、E五种元素,原子序数依次增大,A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等。则下列说法正确的是
A.B与A只能组成BA3化合物
B.C、D、E形成的化合物与稀硫酸可能发生氧化还原反应
C.A、B、C形成的化合物一定不能发生水解反应
D.E的氧化物对应的水化物一定有强的氧化性
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省台州市高一下学期第一次月考化学试卷(解析版) 题型:选择题
在乙烯、乙醛(C2H4O)组成的混合物中,氢元素的质量分数是9%,则氧元素的质量分数为
A.16% B.37% C.48% D.无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com