
【题目】下列既是氧化还原反应,又是吸热反应的是( )
A.二氧化碳与赤热的炭反应生成一氧化碳
B.葡萄糖在人体内氧化
C.锌粒与稀H2SO4反应制取H2
D.Ba(OH)28H2O与NH4Cl反应
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合如图的是( )
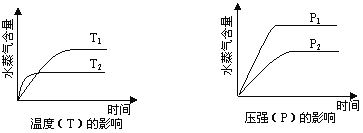
A. CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g)ΔH<0
CO(NH2)2(s)+H2O(g)ΔH<0
B. CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH>0
CO(g)+H2O(g) ΔH>0
C. CH3CH2OH(g)![]() CH2=CH2(g)+H2O(g) ΔH>0
CH2=CH2(g)+H2O(g) ΔH>0
D. 2C6H5CH2CH3(g)+O2(g)![]() 2C6H5CH=CH2(g)+2H2O(g) ΔH<0
2C6H5CH=CH2(g)+2H2O(g) ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水的离子积:25℃时Kw=1×10﹣14,100℃时Kw=1×10﹣12。试回答以下问题.
(1)25℃时,某Na2SO4溶液中c(SO42﹣)=5×10﹣4 molL﹣1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH﹣)=_________.
(2)在100℃时,测得某溶液pH=7,该溶液显_________(填“酸”、“碱”或“中”)性.
(3)将100℃温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合,若所得混合液pH=2,则a:b=________.
(4)某温度时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw=________。
①该温度下( T ℃),将100 mL 0.1 mol·L-1的稀H2SO4溶液与100 mL 0.4 mol·L-1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=____________。
②该温度下(T ℃),1体积的稀硫酸和10体积的NaOH溶液混合后溶液呈中性,则稀硫酸的pH(pHa)与NaOH溶液的pH(pHb)的关系是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用H++OH﹣=H2O来表示的化学反应是( )
A.NaOH溶液与碳酸反应
B.Cu(OH)2与稀硝酸反应
C.Ba(OH)2溶液与稀硫酸反应
D.KOH溶液与稀盐酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)铁在元素周期表中的位置_________。
(2)配合物Fe(CO)n常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)n晶体属于______(填晶体类型)。Fe(CO)n的中心原子价电子数与配体提供电子数之和为18,则n=______ 。Fe(CO)n在一定条件下发生反应:Fe(CO)n(s)![]() Fe(s)+ n CO(g)。已知反应过程中只断裂配位键,则该反应生成物中新形成的化学键类型为___________。
Fe(s)+ n CO(g)。已知反应过程中只断裂配位键,则该反应生成物中新形成的化学键类型为___________。
(3)K3[Fe(CN)6]溶液可用于检验________(填离子符号)。CN-中碳原子杂化轨道类型为_________,C、N、O三元素的第一电离能由大到小的顺序为_______(用元素符号表示)。
(4)铜晶体的晶胞如右图所示。
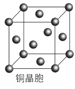
①基态铜原子的核外电子排布式为________________。
②每个铜原子周围距离最近的铜原子数目________。
(5)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如附图所示(黑点代表铜原子)。
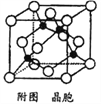
①该晶体的化学式为____________。
②已知该晶体的密度为g.cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为_________pm(只写计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O)简称三盐,白色或微黄色粉末,稍带甜味、有毒。200℃以上开始失去结晶水,不溶于水及有机溶剂。可用作聚氯乙烯的热稳定剂。以铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。

已知:常温下PbSO4的溶解度比PbCO3的溶解度大
请回答下列问题:
(1)步骤①转化的目的是____________,滤液1中的溶质为Na2CO3和_________(填化学式)。
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是___________(任写一条)。其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为__________________。
(3)滤液2中可循环利用的溶质为__________(填化学式)。
(4)步骤⑥合成三盐的化学方程式为_______________________________________(已知反应中元素价态不变)。
(5)简述步骤⑦洗涤沉淀的方法__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的应用错误的是
A.可用氧化铁与铝在高温下反应炼铁B.硫化钠与浓硫酸反应可制备硫化氢
C.铁丝在氯气中燃烧可制得无水三氯化铁D.氧化钙与水反应可用作自热米饭加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用以下方法制取氯气:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,
MnCl2+Cl2↑+2H2O,
(1)用双线桥标出电子转移方向和数目 . (在答题纸上标)
(2)在标准状况下生成的Cl2为11.2L时,参加反应的HCl的物质的量为 , 被氧化HCl的质量为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com