
【题目】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的结构式为 。
(2)Fe2O3是主氧化剂,与Na反应生成的还原产物为 (已知该反应为置换反应),Fe2O3还可用于“铝热法”炼铁,铝热反应在冶金工业上可用于 。
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O,Na2O的电子式为 。
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为:_________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】I. 钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:
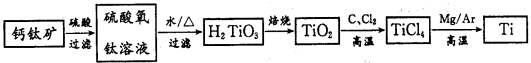
回答下列问题:
(1)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,可知TiCl4为___________晶体。
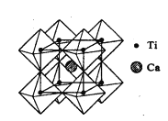
(2)钙钛矿晶体的结构如图所示。钛离子位于立方晶胞的角顶,被____个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被____个氧离子包围。
(3)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:
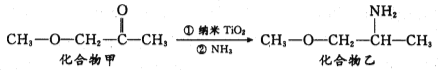
化合物甲中C原子的杂化方式为_______________;化合物乙的沸点明显高于化合物甲,主要原因是_______________________________。
II. 金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(4)镍元素在元素周期表中的位置为 。
(5)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO________FeO(填“<”或“>”);
(6)甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内的O—C—H键角______(填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
(7)Ni的氯化物与氨水反应可形成配合物[Ni(NH3)4]Cl2,2mol该配合物中含有σ键______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰基丙烯酸酯在碱性条件下能快速聚合为 从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:
从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:

已知:
①A的相对分子质量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A 的化学名称为__________________,。
(2)B的结构简式为____________________。其核磁共振氢谱显示为______组峰,峰面积比为_______。
(3)由C生成D的反应类型为_____________。
(4)由D生成E的化学方程式为__________________________________________________________。
(5)G中的官能团有__________、__________、__________。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有___________种。(不含立体结构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡用作媒染剂和有机合成的氯化催化剂,实验室制备四氯化锡的反应、装置示意图和有关信息如下:
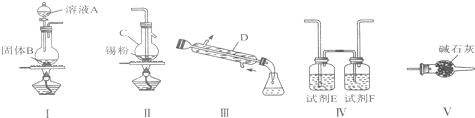
有关信息:
①将金属锡熔融,通入干燥氯气进行反应,生成四氯化锡。
②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃。
⑧暴露于空气中与空气中的水分反应生成白烟,有强烈的刺激性,遇水分解。
回答下列问题:
(1)仪器C的名称是 。
(2)制备无水四氯化锡各装置的连接顺序是( )→( )→( )→( )→( )(填装置序号)。
(3)装置V的作用是 。
(4)若无装置V存在,在装置Ⅲ中除生成SnCl4外,还存在的副产物化学式为 。
(5)若Ⅱ中用去锡粉5.95 g,反应后,Ⅲ中锥形瓶里收集到12.0 g SnCl4,则SnCl4的产率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.氯气通入氯化亚铁溶液中:Cl2+Fe2+=2Cl-+Fe3+
B.钠投入水中:Na+H2O=H2↑+Na++OH-
C.漂白粉的漂白原理:2ClO-+CO2+H2O=CO32-+2HClO
D.用小苏打治疗胃酸过多:HCO3-+H+=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲乙丙丁戊是中学常见的无机物,他们的转化关系如图所示(某些条件和部分产物已略去)。下列说法错误的是
A.若戊为一种强碱且焰色反应为黄色,则反应①②可能都属于氧化还原反应
B.常温下,若丙为无色气体,戊为红棕色气体,则甲、乙是铜和稀硝酸
C.若甲为硫磺燃烧产物,丁为水,则戊可用于干燥甲
D.若甲为浓盐酸,乙为MnO2,则戊可能使品红褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 甲烷中混有少量乙烯,可将混合气体通入盛有酸性高锰酸钾溶液的洗气瓶中除去
B. 在苯中加入酸性KMnO4溶液,振荡并静置后下层液体为紫色
C. 在苯中加入溴的四氯化碳溶液,振荡并静置后下层液体为无色
D. 食物中含有大量的纤维素,可以在人体内直接水解成葡萄糖成为营养物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 L的H2(已折算成标准状况)。甲与水反应也能放出H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状况下的密度为1.25g·L-1。请回答下列问题:
(1)甲的化学式是 ;乙的电子式是 。
(2)甲与水反应的化学方程式是 。
(3)气体丙与金属镁反应的产物是 (用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式 。有人提出产物Cu中可能还混有Cu2O,请设计实验方案验证之 。
(已知:Cu2O + 2H+ = Cu + Cu2+ + H2O)
(5)甲与乙之间 (填“可能”或“不可能”)发生反应产生H2,判断理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com