
| A. | PH3的VSEPR模型为四面体形 | B. | PH3分子中P原子采取sp2杂化 | ||
| C. | PH3分子中P原子上有1个孤电子对 | D. | PH3分子的立体构型是三角锥形 |
分析 A.VSEPR模型为四面体说明该微粒的价层电子对是4,价层电子对=σ 键电子对+中心原子上的孤电子对;
B.价层电子对个数=σ 键+孤电子对个数,PH3杂化轨道数是4,PH3的分子是采用sp3杂化;
C.分子中除了用于形成共价键的键合电子外,还经常存在未用于形成共价键的非键合电子.这些未成键的价电子对叫做孤对电子,PH3中P原子成3个σ键,有一对未成键的孤对电子;
D.PH3的分子是采用sp3杂化,P上连有3个氢,有一对孤对电子,分子构型是三角锥形.
解答 解:A.PH3分子中价层电子对=3+$\frac{5-3}{2}$=4,所以其VSEPR模型为正四面体,故A正确;
B.PH3分子中价层电子对个数=σ键个P数+孤电子对个数=3+$\frac{1}{2}$(5-3×1)=4,所以磷原子采用sp3杂化,故B错误;
C.PH3的P原子最外层满足8电子结构,P上连有3个氢,有一对孤对电子,故C正确;
D.PH3分子中价层电子对个数=σ键个P数+孤电子对个数=3+$\frac{1}{2}$(5-3×1)=4,所以磷原子采用sp3杂化,PH3分子中中心原子上有一对孤电子对,所以分子构型是三角锥形,故D正确;
故选B.
点评 本题以膦为载体考查了物质的结构、化学键等知识点,以氨气分子为例采用知识迁移的方法进行分析解答,注意结合基本概念分析,题目难度中等.


科目:高中化学 来源: 题型:解答题

 ,B:
,B: ,C:
,C: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
 A结构式CH2=CH2
A结构式CH2=CH2查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应的产物Cu2HgI4中,Hg的化合价为+2 | |
| B. | 上述反应中CuI既是氧化剂,又是还原剂 | |
| C. | 上述反应中Hg元素与Cu元素均被氧化 | |
| D. | 上述反应中生成 64gCu时,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4、C6H6 | B. | CH4、CH2O | C. | C2H6、CH3CHO | D. | C3H8、CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若W是单质铁,则Z溶液可能是FeCl2溶液 | |
| B. | 若W是氢氧化钠,则X与Z可反应生成Y | |
| C. | 若W是强氧化性的单质,则X可能是金属铝 | |
| D. | 若W是氧气,则X、Z的相对分子质量可能相差14 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原儿茶醛是制造医药及染料的中间体,可用于制造多种抗菌素和消炎药物.其结构如图:请回答:
原儿茶醛是制造医药及染料的中间体,可用于制造多种抗菌素和消炎药物.其结构如图:请回答: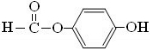 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 镁-过氧化氢燃料电池具有比能量高、安全方便等优点,其结构示意如图所示.关于该电池的叙述正确的是( )
镁-过氧化氢燃料电池具有比能量高、安全方便等优点,其结构示意如图所示.关于该电池的叙述正确的是( )| A. | 电池工作时,H+向正极移动 | |
| B. | 该电池可以在高温下正常工作 | |
| C. | 电池工作时,正极周围溶液的pH将不断变小 | |
| D. | 该电池的总反应式为:Mg+H2O2+H2SO4═MgSO4+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com