
下列各组混合物的分离或提纯方法正确的是( )
A.提纯NaCl和KNO3的混合物中的KNO3:加热蒸发、冷却结晶,过滤
B.除去CO2中混有的少量CO:混合气体依次通过NaOH溶液和浓硫酸
C.除去盐酸溶液中混有的少量CaCl2:加入过量CaCO3粉末,过滤
D.将自来水制成蒸馏水:蒸馏
科目:高中化学 来源:2014-2015学年广东省高二上学期第一次月考理科化学卷(解析版) 题型:选择题
在下列各说法中,正确的是
A.ΔH>0表示放热反应,ΔH<0表示吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省高二上学期第一次月考文科化学卷(解析版) 题型:选择题
标准状况下,32gCH4所占体积约为
A.44.8L B.22.4L C.11.2L D.5.6L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省高二上学期第一次月考文科化学卷(解析版) 题型:选择题
复印机工作时会产生一种腥臭味的气体,该气体只由氧元素组成,其化学式为
A.O2 B.NO2 C.O3 D.N2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省高二上学期第一次月考文科化学卷(解析版) 题型:选择题
3H在月球上储量丰富,4H主要来源于宇宙射线的初级粒子。下列关于3H和4H的说法正确的是
A.两者互为同位素 B.两者互为同素异形体
C.两者为同一种核素 D.两者具有相同的中子数
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省第一学期高一第一次月考化学试卷(解析版) 题型:选择题
下列有关阿佛加德罗常数(NA)的说法错误的是( )
A.32gO2所含的原子数目为NA
B.0.5molH2O含有的原子数目为1.5NA
C.1molH2O含有的H2O分子数目为NA
D.0?5NA个氯气分子的物质的量是0.5mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省广州市高一上学期期中化学试卷(解析版) 题型:实验题
(17分)科学探究
某学习小组根据图中所示的电解水原理进行实验,并对实验得到的与查阅资料获得的数据进行处理、分析,请与他们一起进行探究。请按要求填写。

(1)观察不同时间试管内的H2和O2体积的比值均约为 。
(2)假设电解了1.8g H2O,根据电解水的化学方程式计算生成H2、O2的质量,计算过程如下:
并填表如下:
| 质量g | 物质的量mol | H2 和O2物质的量的比 |
H2 |
|
|
|
O2 |
|
|
根据该实验的观察与推算初步得到关于气体体积规律的一个结论是:在相同的温度和压强下,
(3)下表列出了一些物质的体积
条件 | 物质 | 1 mol物质的体积 |
0℃101kPa | H2 | 22.3 L |
O2 | 22.4 L | |
CO2 | 22.4 L | |
25℃101kPa | H2 | 24.4L |
O2 | 24.5L | |
CO2 | 24.5L |
根据上表数据,得出的结论是(至少写出三点)
①在相同的温度压强下,
②
③
④
(4)请从微观的角度解释气体体积变化规律的原因:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省广州市高一上学期期中化学试卷(解析版) 题型:选择题
下列实验操作中正确的是
A.不慎将浓碱溶液溅到眼睛里,应立即用大量水冲洗,再涂上硼酸溶液中和
B.从试剂瓶倾倒液体时,试剂瓶标签面向手心
C.用酒精灯直接给烧杯内的液体加热
D.用托盘天平称量5.85g的NaCl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二10月月考化学试卷(解析版) 题型:填空题
在一容积为2 L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)  2NH3(g)ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
2NH3(g)ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
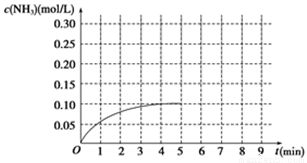
(1)根据图示,计算从反应开始到平衡时(4min末),平均反应速率v(NH3)为____________________;
(2)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为____________(填序号);
a.0.20 mol/L b.0.12 mol/L c.0.10 mol/L d.0.08 mol/L
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡______________移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________(填“增大”、“减小”或“不变”);
(4)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在图中画出第5分钟末到达新平衡时NH3浓度的变化曲线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com