
����Ŀ��I.ij�βɼ�������Ʒ��ÿ��һ��ʱ��ⶨһ��pH���õ��������£�
ʱ�� | ��ʼ | 8Сʱ | 16Сʱ | 24Сʱ | 32Сʱ | 40Сʱ | 48Сʱ |
pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(1)����ʱ����ˮ��Ʒ����_______________�����ǿ���������������䡱����
���Ա仯��ԭ��_________________________________���û�ѧ����ʽ��ʾ����
II.����β��(�������ࡢCO��SO2��NO������)�dz��п�������ȾԴ��ұ���ķ���֮һ������������������װһ������ת������(�ò����ٺϽ�������)�������ص���ʹCO��NO��Ӧ�����ɿɲ��������̬����ѭ���������壬����ʹ������ȼ�ռ�SO2��ת����
(2) д��һ����̼��һ��������Ӧ�Ļ�ѧ����ʽ��__________________________��
(3) �ڡ���ת������ת�������������CO2��SO2�����в��ܼ������������������____��
A.KMnO4��Һ B.ʯ��ˮ C.BaCl2��Һ D.Ʒ����Һ
(4) ��Ч���ٳ�����Ⱦ�ķ���������____________
A. ��������Դ B. ʹ�õ綯�� C. ֲ������ D. ���Ϻ������
���𰸡� ��ǿ 2SO2��2H2O��O2= 2H2SO4��2H2SO3��O2==2H2SO4 2CO��2NO![]() 2CO2��N2 BC ABC
2CO2��N2 BC ABC
��������(1)������Ʒ���ã�������ǿ��ԭ���Ƿ��ù����У����귢���ķ�ӦΪ2H2SO3+O2=2H2SO4��������Ʒ�е�H2SO3��������H2SO4��ʹ��Һ��������ǿ��
(2)�ڴ������£�һ��������һ����̼��Ӧ���ɶ�����̼�͵���������ʽΪ��2NO+2CO![]() 2CO2+N2��
2CO2+N2��
(3)A��KMnO4��Һ����CO2��Ӧ������SO2��Ӧ��5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4�����Լ��𣬹�A����B��SO2��CO2����ʹ�����ʯ��ˮ����ǣ�������ͬ�������𣬹�B��ȷ��C��������̼��SO2������ʹBaCl2��Һ ����ǣ������Լ��𣬹�C��ȷ��D�������������Ư������ʹƷ����ɫ����������̼����ʹƷ����ɫ������Լ��𣬹�D����ѡBC��
(4)A������ȼ�յIJ�����ˮ���Ի���������Ⱦ�ģ��ܿ��Ƴ��п�����ȾԴ����A��ȷ��B��ʹ�õ綯������������Կ�������Ⱦ�����ʣ��ܿ��Ƴ��п�����ȾԴ����B��ȷ��C��ֲ�����ֿ��Ծ���������������������C��ȷ��D������������ڿ������м���Σ�յIJ�������Ⱦ��������ģ�ƽʱ���������Dz��˴��ģ����Ǵ�Դͷ�Ͽ��ƿ�����ȾԴ����D����ѡABC��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��700��ʱ��H2��g����CO2��g��![]() H2O��g����CO��g�������¶��£��ڼס��ҡ������������ܱ������У�Ͷ��H2��CO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��v (H2O)Ϊ0.025 mol/��L��min���������жϲ���ȷ���ǣ� ��
H2O��g����CO��g�������¶��£��ڼס��ҡ������������ܱ������У�Ͷ��H2��CO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��v (H2O)Ϊ0.025 mol/��L��min���������жϲ���ȷ���ǣ� ��
��ʼŨ�� | �� | �� | �� |
C��H2��/mol/L | 0.1 | 0.2 | 0.2 |
C��CO2��/mol/L | 0.1 | 0.1 | 0.2 |
A��ƽ��ʱ������CO2��ת���ʴ���50��
B������Ӧƽ��ʱ������c��CO2���Ǽ��е�2��
C���¶�����800����������Ӧƽ�ⳣ��Ϊ25/16��������ӦΪ���ȷ�Ӧ
D�������������䣬����ʼʱ���������г���0.10mol/L H2��0.20 mol/L CO2������ƽ��ʱc (CO)���Ҳ�ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)���������ڰ�ˮ�γ�[Ni(NH3)6]SO4��ɫ��Һ��[Ni(NH3)6]SO4�������ӵĿռ乹����________��
(2)��[Ni(NH3)6]2����Ni2����NH3֮���γɵĻ�ѧ����Ϊ________���ṩ�µ��ӶԵijɼ�ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������з�����Ӧ��X��3Y![]() 2Z���÷�Ӧ������������Z����̬����Z��ƽ�������е����������Z%�����¶���T����ѹǿ��P���Ĺ�ϵ��ͼ�������ж���ȷ����
2Z���÷�Ӧ������������Z����̬����Z��ƽ�������е����������Z%�����¶���T����ѹǿ��P���Ĺ�ϵ��ͼ�������ж���ȷ����
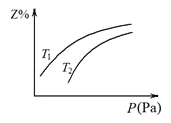
A��T1����T2
B��Yһ������̬
C�������¶ȣ��÷�Ӧ�Ļ�ѧƽ�ⳣ������
D����n��X��:n��Y��:n��Z����1:3:2ʱ����Ӧһ���ﵽƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1965���ҹ���ѧ�Һϳ��˽ᾧţ�ȵ��أ�������
A�������� B����֬���� C��������ά D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)д��Ũ������ľ̿���ڼ��������·�Ӧ�Ļ�ѧ����ʽ _��
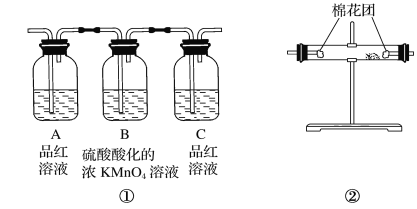
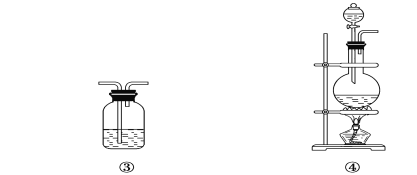
��2��������ͼ��ʾ��װ�����һ��ʵ�飬��֤������Ӧ�������ĸ��ֲ����Щװ�õ�����˳��(����������������ҵ�����)��________��________��________��________(��װ�õı��)��
��3�������������װ�õ�������
��4��ʵ��ʱ�ɹ۲쵽װ������Aƿ����Һ��ɫ��Cƿ����Һ����ɫ��Aƿ��Һ��������________��Bƿ��Һ��������________��Cƿ��Һ��������________��
��5��װ���������ӵĹ���ҩƷ��________������֤�IJ�����________��
��6��װ��������ʢ��Һ��________������֤�IJ�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ñ��͵�FeCl3��Һ��ȡFe��OH��3���壬��ȷ�IJ����ǣ� ��
A.��FeCl3��Һ��������ˮ��
B.��FeCl3��Һ������ˮ�У������ػ�ɫҺ��
C.��FeCl3��Һ���˷�ˮ�У���������������ɺ��ɫҺ��
D.��FeCl3��Һ���˷�ˮ�У���������������ɺ��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ�к��У���Na������Ba2������Cl������Br������SO![]() ����SO
����SO![]() �е�һ�ֻ��֣����ν�������ʵ�飬��ÿ�����ӵ��Լ����������۲쵽���������±���ʾ��
�е�һ�ֻ��֣����ν�������ʵ�飬��ÿ�����ӵ��Լ����������۲쵽���������±���ʾ��
���� | �� �� | �� �� |
�� | ��pH��ֽ���� | ��Һ��pH����7 |
�� | ����Һ�еμ���ˮ���ټ���CCl4������ | CCl4��ʳ�ɫ |
�� | ���������Һ�м���Ba(NO3)2��Һ��ϡHNO3 | �а�ɫ�������� |
�� | ���ˣ�����Һ�м���AgNO3��Һ��ϡHNO3 | �а�ɫ�������� |
����ʵ�������ȷ����( )
A���϶����е������Ǣ٢ܢ�
B���϶�û�е������Ǣڢ�
C�����ܺ��е������Ǣ٢ڢ�
D������ȷ���������Ǣ٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������H++OH��=H2O��ʾ�Ļ�ѧ����ʽ�ǣ� ��
A.����������Һ����ᷴӦ
B.�������������ᷴӦ
C.�������������ᷴӦ
D.��������������������Һ��Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com