
【题目】根据要求回答下列有关问题。
(1)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) H=-28.5kJ/mol,冶炼铁反应的平衡常数表达式K=____________,温度升高后,K 值________(填“增大”、“不变”或“减小”)。
2Fe(s)+3CO2(g) H=-28.5kJ/mol,冶炼铁反应的平衡常数表达式K=____________,温度升高后,K 值________(填“增大”、“不变”或“减小”)。
(2)已知:①Fe2O3(s)+3C(石墨) = 2Fe(s)+3CO(g) H1= +489.0kJ/mol
②Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) H2= -28.5kJ/mol
2Fe(s)+3CO2(g) H2= -28.5kJ/mol
③C(石墨)+ CO2(g) = 2CO(g) H3= akJ/mol ,
则a=__________kJ/mol。
(3)在T℃时,反应Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。
2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。
Fe2O3 | CO | Fe | CO2 | |
始态mol | 1.0 | 1.0 | 1.0 | 1.0 |
①平衡时CO 的转化率为_______。
②下列情况标志反应达到平衡状态的是________(填字母)。
a.容器内气体密度保持不变
b.容器内气体压强保持不变
c.CO的消耗速率和CO2的生成速率相等
【答案】 K= c(CO2)3 /c(CO)3 减小 +172.5 60% a
【解析】(1)根据平衡常数的概念,由于固体物质或纯液体的浓度是常数,不能写入表达式,则高炉炼铁的平衡常数K=c3(CO2)/c3(CO);升高温度,平衡向吸热的方向移动,结合方程式:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) H=-28.5kJ/mol,即平衡向左移动,故平衡常数减小;(2)根据盖斯定律:(①-②)÷3=(△H1-△H2)÷3= +172.5 kJ/mol;(3)①起始时甲容器中c3(CO2)/c3(CO)=1.03/1.03=1<64,说明该反应一定从正反应方向开始进行,反应物浓度减小,生成物浓度增大,直到达到新的平衡,设CO的平衡转化率为x,则:
2Fe(s)+3CO2(g) H=-28.5kJ/mol,即平衡向左移动,故平衡常数减小;(2)根据盖斯定律:(①-②)÷3=(△H1-△H2)÷3= +172.5 kJ/mol;(3)①起始时甲容器中c3(CO2)/c3(CO)=1.03/1.03=1<64,说明该反应一定从正反应方向开始进行,反应物浓度减小,生成物浓度增大,直到达到新的平衡,设CO的平衡转化率为x,则:
Fe2O3(s) + 3CO(g) ![]() 2Fe(s) + 3CO2(g)
2Fe(s) + 3CO2(g)
起始浓度/ mol·L-1 0.5 0.5
变化浓度/ mol·L-1 0.5x 0.5x
平衡浓度/ mol·L-1 0.5-0.5x 0.5+0.5x
K=c3(CO2)/c3(CO)="(" 0.5+0.5x)3/(0.5-0.5x)3=64
( 1+x)3/(1-x)3=64,则( 1+x)/(1-x)=4,1+x=4-4x,5x=3,x=0.6或60%
②混合气体的密度=混合气体的总质量/容器的容积,由于反应物和生成物中都有固体物质参加,且平衡前混合气体的总质量会增大,只有平衡时混合气体的总质量才保持不变,密度才不变,a正确;正反应是气态物质体积保持不变的反应,则反应前后气态物质的物质的量保持不变,则平衡前后气体的压强不变,b错误;CO的消耗速率和CO2的生成速率均为正反应速率,c错误。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是( )
A. 在强碱溶液中:Na+、K+、AlO2﹣、CO32﹣
B. 在pH=0的溶液中:K+、Fe2+、Cl﹣、NO3﹣
C. 在含大量Fe3+的溶液中:NH4+、Na+、Cl﹣、SCN﹣
D. 在c(H+)=10﹣13mol/L的溶液中:NH4+、Al3+、SO42﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验兴趣小组利用下列实验装置探究氯气与过量氨气反应的实验,有关说法不正确的是
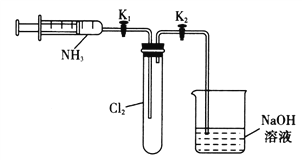
A. 打开K1,关闭K2,将注射器的活塞往外拉一小段,然后松开,活塞复原,说明装置气密性良好
B. 打开K1,推动注射器的活塞使过量的氨气与氯气混合时,产生大量的白色烟雾
C. 充分反应后,关闭K1,打开K2,可观察到烧杯中的溶液会倒吸至试管内
D. 实验室制备氨气和氯气可以用同一套发生装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列数量的各物质中,含原子个数最多的是( )
A.1mol HClB.3.01 x 1023 个碘分子C.12g 12CD.0.5mol CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是( )
A. 现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
B. 28 g CO和22.4 L CO2中含有的碳原子数一定相等
C. 标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D. a g Cl2中有b个氯原子,则阿伏加德罗常数NA的数值可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸锶主要用于彩电显像管的荧屏玻璃和特种玻璃等的制造,通常由天青石矿(主要成分为SrSO4,还含有钡等杂质)制备,制备流程如图所示:
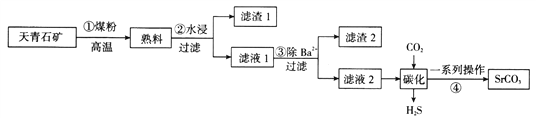
已知:i.锶在“滤液1”“滤液2”中均主要以Sr(HS)2、Sr(OH)2形式存在
ii.SrSO4、BaSO4的KSP分别是3.2×10-7、1.0×10-10
回答下列问题:
(1)步骤①反应:SrSO4+2C![]() SrS+2CO2↑,若在标准状况下产生3.36 LCO2,则转移电子数为__________________。
SrS+2CO2↑,若在标准状况下产生3.36 LCO2,则转移电子数为__________________。
(2)写出步骤②中“水浸”主要反应的化学方程式:________________________。步骤②“过滤”操作需要的主要玻璃仪器为________________________。
(3)上述生产工艺的优点是质量好、成本低,但从环保角度考虑该工艺生产存在明显的缺点是______________________________________________________。
(4)若向含有Sr2+、Ba2+的“滤液1”中滴加稀硫酸,当两种沉淀共存时,c(Sr2+):c(Ba2+)=________________。
(5)写出“碳化”过程中发生反应的化学方程式:_______________________________。
(6)某生产企业用a kg的天青石矿(含SrSO4:40%)制备,最终得到b kg碳酸锶产品,产率为______________(用含a、b的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉和纤维素不属于同分异构体的原因是 ( )
A. 组成的元素不同 B. 物理性质、化学性质不同
C. 组成的单糖单元数不相同 D. 分子结构不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com