
已知25℃时有关物质的电离平衡常数:
| 弱酸 | CH3COOH | 苯酚 | H2CO3 |
| 电离平衡常数 | 1.75×l0–5 | 1.1×l0–10 | K1=4.4×l0–7 K2=4.7×l0–11 |
下列叙述错误的是
A.等物质的量浓度的各溶液pH关系为:
pH(C6H5ONa)>pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa)
B.向苯酚钠溶液中通入少量CO2气体反应为:C6H5O– +H2O + CO2 →C6H5OH +HCO3-
C.等物质的量浓度的苯酚稀溶液与 NaOH稀溶液等体积混合后溶液中:
c(Na+)>c(C6H5O–)>c(OH–)>c(H+)
D.NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +2c(CO32–)
【答案】A
【解析】
试题分析:根据电离平衡常数可以推出弱酸酸性的强弱,CH3COOH > H2CO3 > 苯酚 > HCO3-,根据越弱越水解,对应的弱酸的盐溶液PH越大,得出等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(C6H5ONa)>pH(NaHCO3)>pH(CH3COONa),A错误;根据强酸制弱酸,向苯酚钠溶液中通入少量CO2气体反应为:C6H5O– +H2O + CO2 →C6H5OH +HCO3-,B正确;等物质的量浓度的苯酚稀溶液与 NaOH稀溶液等体积混合,恰好反应生成苯酚钠,苯酚钠是强碱弱酸盐,会水解显碱性,所以等物质的量浓度的苯酚稀溶液与 NaOH稀溶液等体积混合后溶液中:c(Na+)>c(C6H5O–)>c(OH–)>c(H+),C正确 ;根据电荷守恒,NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +2c(CO32–),D正确。
考点:考查弱电解质强弱的比较,盐的水解的基本知识,电荷守恒等知识。


科目:高中化学 来源: 题型:
对于硝酸的物理性质,下列叙述中,不正确的是( )
A.可以与水以任意比互溶
B.不易挥发
C.有刺激性气味
D.质量分数在95%以上的硝酸为发烟硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对阿伏加德罗常数的叙述中,正确的是( )
①阿伏加德罗常数就是6.02×1023 mol-1
②阿伏加德罗常数为1 mol指定粒子的粒子数
③阿伏加德罗常数为12 g碳所含的碳原子数
④阿伏加德罗常数用符号NA表示,其值约为6.02×1023 mol-1
A.①② B.①③ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和生活中有着重要的应用。下列说法正确的是
A.硫酸钡在医学上用作钡餐,Ba2+对人体无毒
B. “光化学烟雾”、“雾霾天气”、“温室效应”的形成都与氮氧化物无关
C.“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料
D.明矾[KAl(SO4)2·12H2O]水解时产生具有吸附性的胶体粒子,可作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在相应的条件下一定能大量共存的是
A.在碱性溶液中:HCO3-、K+、C1-、Na+
B.与铝粉反应放出氢气的无色溶液中:NO3-、K+、Na+、SO42-
C.在c(H+)/c(OH-)==1×1013的溶液中:NH4+、Br-、C1-、K+
D.通有SO2的溶液中: Ca2+、C1-、NO3-、A13+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语的相关表述正确的是
A.H+(aq)+OH-(aq)=H2O(l) △H=-a kJ/mol,故1 mol NaOH固体与足量的稀盐酸反应,放出热量为a kJ
B.因CuSO4·5H2O(s)=CuSO4(s)+5H2O(1) △H=+b kJ/mol,故1 mol CuSO4(s)溶于足量水时,放出热量为b kJ
C.因氢气的燃烧热为c kJ/mol,故电解水的热化学方程式为:2H2O(1)=2H2(g)+O2(g)△H=+c kJ/mol
D.因N2(g)+3H2(g) 2NH3(g) △H=-d kJ/mol,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于d kJ
2NH3(g) △H=-d kJ/mol,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于d kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示装置是化学实验中常见的仪器,它除用于洗气外,还有其他用途:

(1)医院里给病人输氧时,往往在氧气钢瓶与病人呼吸面具之间安装盛有水的该装置,用 于观察气泡产生的情况,以便调节供氧速率, 此时氧气应从 (填标号,下同)管口导入。
(2)实验室用MnO2与浓HCl反应制Cl2的实验中,在将生成的Cl2通入NaOH溶液之前,先将Cl2从该装置 管口导入,此时,该装置所起的作用是防止NaOH溶液倒流入反应器。
(3) 当用此装置收集NO时,应采取的主要操作步骤是:
① ;
② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:KClO3+C+S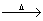 KCl+CO2 ↑+SO2↑,下列判断不正确的是
KCl+CO2 ↑+SO2↑,下列判断不正确的是
A.若反应中C和S的质量比为3:4,则n(KClO3):n(CO2)为1:1
B.若反应中C和S的质量比为3:16,则n(KClO3):n(CO2)为2:1
C.SO2通人NaHCO3溶液产生CO2,可证明非金属性S强于C
D.KClO3与SO2在强酸性溶液中反应制得ClO2,可证明SO2的还原性强于ClO2
查看答案和解析>>
科目:高中化学 来源: 题型:
钛(Ti)因为具有神奇的性能越来越引起人们的关注。常温下钛不和非金属、强酸反应。红热时,却可与常见的非金属单质反应。钛是航空、军工、电力等方面的必需原料。地壳中含钛矿石之一是金红石(TiO2),目前大规模生产钛的方法是:第一步:金红石、碳粉混合,在高温条件下通入Cl2制得TiCl4和一种可燃性气体,该反应的化学方程式为______________________________,该反应的还原剂是________。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)写出此反应的化学方程式:_____________________________________________。
(2)简述从上述所得产物中获取金属钛的步骤___________________________ _______________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com