
【题目】
(1)氨气是化学实验室常需制取的气体。实验室制取氨气通常有两种方法:
方法一 固体氢氧化钙与氯化铵共热
方法二 固体氢氧化钠与浓氨水反应
①下面的制取装置图中,方法一应选用装置________(填“A”或“B”,下同),方法二应选用装置________。
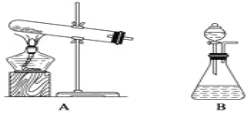
②写出加热NH4Cl和Ca(OH)2制取NH3的反应方程式:
________________________________________________________________________。
③在制取后,如果要干燥氨气,应选用的干燥剂是________,收集氨气的方法是
A.浓硫酸
B.碱石灰
C.五氧化二磷
D.向上排空气法
E.排水法
F.向下排空气法
④检验是否收集满氨气的方法是____________________________________
(2)请观察如图装置,回答下列问题:
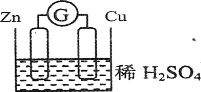
①负极是 ,发生 反应(填氧化或还原)
②正极的电极反应式:
③该装置是一种把 的装置,当导线中有0.2 mol e-发生转移时,求参加氧化反应的物质的物质的量为
【答案】(1)①A ;B
②2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O
③B; F
④用湿润的红色石蕊试纸放在试管口,看试纸是否变蓝,变蓝则收集满(正确都得分)
(2)① Zn;氧化
②2H+ +2e-= H2↑
③化学能转变为电能;0.1mol
【解析】
试题分析:①方法一:实验室用氯化铵和氢氧化钙在加热条件下制备氨气,利用固体+固体加热制备气体选择气体发生装置为A;方法二:实验室用固体氢氧化钠与浓氨水反应制取氨气,利用固体+液体不加热制备气体选择气体发生装置为B。
故答案为:A;B
②实验室用氢氧化钙和氯化铵在加热条件下制备氨气,反应方程式为:2NH4Cl+Ca(OH)2![]() CaCl2+2H2O+2NH3↑。
CaCl2+2H2O+2NH3↑。
故答案为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
③由于氨气属于碱性气体,所以在制取后如果要干燥氨气,应选用碱性干燥剂碱石灰,即选B;氨气极易溶解于水且密度比空气小,所以收集氨气的方法是向下排空气法,即选F。
故答案为:B;F;
④氨气为碱性气体,与水反应生成NH3H2O,电离子出OH-离子,溶液呈碱性,检验时可用用蘸有浓盐酸的玻璃棒靠近试管口,如果产生白烟,则证明为氨气,或用湿润的红色石蕊试纸靠近试管口,如果 试纸变蓝,则证明是氨气氨气。
故答案为:用蘸有浓盐酸的玻璃棒靠近试管口,如果产生白烟,则证明为氨气;或用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则证明是氨气。
(2)①电极材料为Cu和Zn,Zn较活泼,作原电池的负极,失去电子而被氧化,故答案为:Zn;氧化;
②C为该原电池的正极,正极上发生还原反应,电极反应式为:2H++2e-=H2↑。
故答案为:2H++2e-=H2↑;
③该装置是一种把化学能转变为电能的装置,属于原电池装置;该原电池工作时,正极反应为2H++2e-=H2↑,负极反应为Zn-2e-=Zn2+,所以当导线中有0.2mole-发生转移时,求参加氧化反应的Zn的物质的量为0.1mol。
故答案为:化学能转变为电能;0.1mol。


科目:高中化学 来源: 题型:
【题目】镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
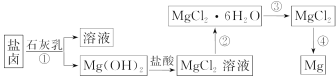
回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是___ __ __ __ __ ___。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有__ ___ _溶液(填写化学式)的烧杯中,充分搅拌后经__ _ __ _ __、__ _ __ __ __(填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:

其中装置A的作用是___ ___ __ _ __ __ ___ __ __。
(4)写出过程④中发生反应的化学方程式___ __ __ __ __ ___。
(5)金属Mg在CO2中完全燃烧生成MgO和C,下列说法正确的是___ ___。
A.碳单质只存在金刚石和石墨两种同素异形体
B.Mg、MgO中镁元素微粒半径:r(Mg2+) > r(Mg)
C.在该反应条件下,Mg的还原性强于C的还原性
D.该反应中化学能全部转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮及其化合物的性质具有极为重要的意义。
(1) NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_____________________________
(2)在含Cu+离子的酶的活化中,亚硝酸根 (NO2-)离子可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式 。
(3)将38.4 g铜与150mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L,请回答:
① NO2的体积为____________L。
②若铜与硝酸刚好反应完全,则原硝酸溶液的浓度为____________molL-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质有广泛用途。
(1)C8H8O3的某一同分异构体尼泊金酯的结构简式为:![]() 。
。
①下列对尼泊金酯的判断错误的是 。
a.能发生水解反应
b.能与FeCl3溶液发生显色反应
c.分子中所有原子都在同一平面上
d.能与浓溴水反应产生白色沉淀。
②尼泊金酯与足量NaOH溶液在一定条件下反应的化学方程式是 。
(2)C8H8O3的另一种同分异构体甲的结构简式为:![]() 。
。
①甲中含氧官能团的名称为:羧基和 。
②甲在一定条件下跟足量的Na反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把l00mL2.0 mol/L CuSO4溶液和l00 mL l.0 mol/LH2SO4溶液混合(假设混合后溶液的体积等于混合前两种溶液的体积之和)。计算
(1)混合溶液中CuSO4的物质的量浓度。
(2)混合溶液中SO42-的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、环境等社会实际密切相关。下列叙述正确的是
A. “滴水石穿、绳锯木断”不涉及化学变化
B. 明矾净水的原理和消毒液消毒的原理不相同
C. 氟利昂作制冷剂会加剧雾霾天气的形成
D. 汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃C7H8是一种重要的有机化工原料,研究部门以它为初始原料设计出如下
转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,F是一种功能高分子,链节组成为(C7H5NO)。
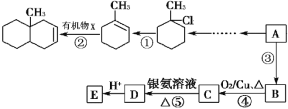
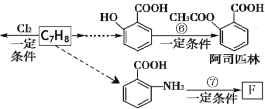
已知:(ⅰ) ![]()
(ⅱ)![]() (苯胺,易被氧化)
(苯胺,易被氧化)
(1)反应①的反应类型是 ,反应⑥的反应类型是 。
(2)反应③的反应条件为 ;有机物X的结构简式为 。
(3)鉴别B和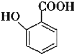 不可选用的试剂有 (填标号)。
不可选用的试剂有 (填标号)。
A.FeCl3溶液 b.浓溴水 C.Na d.NaHCO3溶液
(4)写出反应⑤的化学方程式: ;
若F为高分子化合物,则反应⑦的化学方程式为 。
(5)根据已有知识并结合相关信息,写出以芳香烃C7H8为原料制备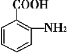 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下(已知
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下(已知![]() 容易被氧化剂氧化):
容易被氧化剂氧化):![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)、室温下,将1.000mol/L盐酸滴入20.00mL 1.000 mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。

(1)a点由水电离出的c(H+)=__________。
(2)d点溶液温度最高的原因是__________ 。
(II)电离常数是衡量弱电解质电离程度强弱的物理量。已知:化学式电离常数(25℃)HCN K=4.9×10-10,CH3COOH K=1.8×10-5,H2CO3 K1=4.3×10-7、K2=5.6×10-11,一氯乙酸K=1.4×10—3
(3)25℃时,有等浓度的:①NaCN溶液,②Na2CO3溶液,③CH3COONa溶液,三溶液的pH由大到小的顺序为________________________。(填序号)
(4)向NaCN溶液中通入少量的CO2,发生反应的化学方程式为_________________。
(5)下图中可以描述乙酸(甲曲线)和一氯乙酸(乙曲线)在水中的电离度与浓度关系的是( )
A.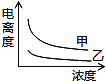 B.
B. C.
C. D.
D.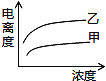
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)光束通过Fe(OH)3胶体,可看到光亮的通路,这种现象叫________;
(2)19g某二价金属的氯化物ACl2中含有0.4mol Cl-离子,求ACl2的摩尔质量________
(3)在标准状况下,测得4.2g气体A的体积是3360mL,则A可能是什么气体________
(4)在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:CO2和CO的体积之比是________。
(5)在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为1.18 g·cm-3。所得盐酸物质的量浓度分别是________
(6)现有以下物质:①NaCl晶体 ②盐酸 ③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧浓H2SO4 ⑨KOH固体;以上物质中属于电解质的是________
(7)Ca(HCO3)2溶液与少量氢氧化钠溶液混合的离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com