
19g某二价金属的氯化物ACl2中含有0.4mol Cl-离子,ACl2的摩尔质量是 g/mol,相对分子质量是 ,A的相对原子质量是 。
科目:高中化学 来源: 题型:
常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通CO2 气体,只能生成HX和NaHCO3;往NaY溶液中通入CO2则生成HY和Na2CO3。有关叙述正确的是
A.酸性由强至弱:HX > HY > H2CO3
B.结合H+的能力:Y― > CO32― >X― > HCO3―
C.溶液物质的量浓度相同时碱性:NaX > Na2CO3 > NaY > NaHCO3
D.NaX溶液中通入足量CO2后:c(X―) >c(Na+) >c(HCO3―) >c(OH―)
查看答案和解析>>
科目:高中化学 来源: 题型:
0.5L, 1mol/L FeCl3溶液中的Cl-的物质的量浓度为
A.3 mol/L B. 1.5 mol/L C.1 mol/L D. 0.5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
100mL0.3mol/LNa2SO4溶液和50mL0.2mol/L Al2(SO4)3溶液混合后(忽略体积变化),溶液中SO42-的物质的量浓度为
A.0.2mol/L B.0.25mol/L C.0.40mol/L D.0.50mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
取1.43g Na2CO3•10H2O溶于水配成100ml溶液,求:
(1)Na2CO3物质的量浓度
(2)Na+ 物质的量浓度
(3)取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.004mol/L,求加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年6月11日,我国“神十”载人航天飞船发射取得圆满成功。火箭发射时燃料燃烧的反应为:2 N2H4(g)+ 2NO2(g)= 3N2(g)+4H2O(l)△H=akJ/mol, 关于此反应的下列说法中正确的是
A.a>0 B.每生成1mol水,转移8mol电子
C.氧化产物与还原产物的质量比为2:1 D.N2H4是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
1.6mol CH4与Cl2发生取代反应,待反应完成后测得4种氯代物的物质的量依次增大0.2mol,则参加反应的Cl2为( )
A、5mol B、2mol C、2.5mol D、4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验 。
①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。
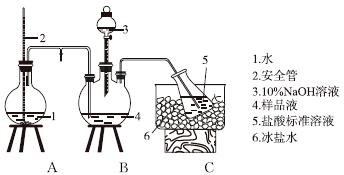
氨的测定装置(已省略加热和夹持装置)
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是__________________________________________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用________式滴定管,可使用的指示剂为________。
(3)样品中氨的质量分数表达式为________。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将________(填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是____________________;滴定终点时,若溶液中c(Ag+)=2.0×10-5 mol·L-1,c(CrO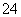 )为________mol·L-1。[已知:Ksp(Ag2CrO4)=1.12×10-12]
)为________mol·L-1。[已知:Ksp(Ag2CrO4)=1.12×10-12]
(6)经测定,样品X中钴、氨和氯的物质的量之比为1∶6∶3,钴的化合价为________,制备X的化学方程式为______________________________________;X的制备过程中温度不能过高的原因是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com