
【题目】根据下列图示所得出的结论正确的是( )
甲 乙
乙
丙 丁
丁
A. 图甲是在不同温度下三个恒容容器中反应2H2(g)+CO(g)CH3OH(g) ΔH<0的平衡曲线,曲线X对应的温度相对较高
B. 图乙是一定温度下三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线,a点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-)
C. 图丙为MOH和ROH两种一元碱水溶液在常温下分别加水稀释时pH的变化曲线,可知ROH是强碱
D. 图丁为两个容器中在不同的压强下各投入1 mol CH4和1 mol CO2所发生反应CH4(g)+CO2(g)2CO(g)+2H2(g)的平衡曲线,N点化学平衡常数K=1
【答案】BC
【解析】
应用平衡移动原理,分析外因对化学平衡、沉淀溶解平衡、电离平衡的影响,判断由图象得出的结论是否正确。
A项:在图甲中作任一垂线,与三曲线各有一交点,表明在反应物比例相同时,X曲线对应温度下CO平衡转化率较高。因反应的ΔH<0,故X曲线对应温度较低,A项错误;
B项:过a点作垂线,与MgCO3直线有交点(饱和溶液)。可见,在c(CO32-)相同时,a点溶液中c(Mg2+)比饱和溶液中的小,为不饱和溶液。a点时-lgc(Mg2+)> -lgc(CO32-),则c(Mg2+)<c(CO32-),B项正确;
C项:图丙中ROH加水稀释10倍、100倍或1000倍时,溶液pH减小1、2或3,则ROH是强碱,C项正确;
D项:化学平衡常数只与温度有关,N点的平衡常数可用M点计算。平衡时CH4(g)、CO2(g)的浓度都是0.5mol/L,CO(g)、H2(g)的浓度都是1 mol/L,则K=4,D项错误。
本题选BC。


科目:高中化学 来源: 题型:
【题目】氯氨铂是一种治疗癌症的常用化学药物,具有较高疗效。其中的金属Pt(铂元素)是原子序数为78(质量数为195)的原子,则Pt的中子数与质子数之差是
A.117B.78C.39D.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机分子中,所有的原子不可能处在同一平面的是( )
A. CH2=CH-CNB. CH2=CH-CH=CH2
C. 苯乙烯D. 2-甲基-1,3-丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成一种用于合成γ分泌调节剂的药物中间体,其合成的关键一步如图。

下列有关化合物A、B的说法正确的是( )
A. A→B的反应为取代反应
B. A分子中所有碳原子一定在同一平面上
C. A、B均不能使酸性KMnO4溶液褪色
D. B与足量H2完全加成的产物分子中含有4个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组利用以下装置测定某赤铁矿中氧化铁的纯度:向赤铁矿中通入纯净的一氧化碳气体,假设赤铁矿中杂质不参与反应,请回答下列问题

(1)实验开始时,先进行的操作是___(填序号),其目的是____。
①通入一氧化碳 ②加热
(2)实验过程中观察到装置A中玻璃管内发生的现象___;
(3)写出B装置发生的化学反应方程式是____;装置C的作用是___。
(4)从环境保护的角度看本实验存在的缺陷是___。
(5)实验前称量赤铁矿的质量为20g。通入足量的一氧化碳完全反应后B装置总质量增加了13.2g,则赤铁矿中氧化铁的纯度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: 25℃、101 kPa下:① 2 Na(s) + 1/2 O2(g) = Na2O(s) △H1 = - 414 kJ / mol
② 2 Na(s) + O2(g) = Na2O2(s) △H2 = - 511 kJ / mol
下列说法正确的是
A. ①和②产物的阴阳离子个数比不相等
B. ①和②生成等物质的量的产物,转移电子数不同
C. 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D. 25℃、101 kPa下,Na2O2(s) + 2 Na(s) = 2 Na2O(s) △H = -317 kJ / mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物G是合成降糖药格列美酮的重要原料,其可由化合物A经如下步骤合成。

(1)B中的含氧官能团名称为________。
(2)上述转化中属于加成反应的是________。
(3)试剂X的分子式为C9H9ON,写出X的结构简式:__________________。
(4)1 mol化合物F与足量ClSO3H反应,除G外另一产物的物质的量为________。
(5)写出同时满足下列条件的一种有机物分子的结构简式:____________________。
①与D分子相比组成上少1个“CH2”
②与FeCl3溶液发生显色反应
③核磁共振氢谱显示有5种不同化学环境的氢,其峰面积比为3∶2∶2∶2∶2。
(6)已知:① ;②
;② ;③
;③![]() 。请根据已有知识并结合相关信息,写出以乙醛和甲苯为原料制备
。请根据已有知识并结合相关信息,写出以乙醛和甲苯为原料制备 的合成路线流程图(无机试剂任用) ____________________。
的合成路线流程图(无机试剂任用) ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾大晶体,具体流程如下

已知:(1) AlCl3·6H2O易溶于水、乙醇及乙醚;
(2) 明矾在水中的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
(1)步骤Ⅱ中生成Al(OH)3的离子方程式为____________________________________________。
(2)步骤Ⅲ灼烧Al(OH)3所用实验室常用仪器为________,为了提高Al2O3纯度,需________(填操作步骤)。
(3)制备AlCl3·6H2O的工业生产中,胶状固体用酸浸取后,还需要通入HCl气体。通入HCl的作用主要有两点:____________和____________。
(4)已知:在不同温度条件下向一定量的氯化铝溶液中通入HCl气体,通入量对AlCl3·6H2O结晶量和结晶效率的影响如图,请补充完整由胶状固体制备AlCl3·6H2O晶体的实验方案:向胶状固体滴加一定浓度盐酸,直至恰好完全溶解,__________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的有
①乙酸的最简式:CH2O ②聚丙烯的结构简式:![]()
③羟基的电子式:![]() ④丙烷分子的比例模型:
④丙烷分子的比例模型:
⑤四氧化碳分子的电子式: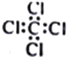 ⑥乙醇的分子式: CH3CH2OH
⑥乙醇的分子式: CH3CH2OH
⑦H2CO3的电离方程式:H2CO3![]() H++HCO3-⑧2-乙基-l,3-丁二烯分子的键线式:
H++HCO3-⑧2-乙基-l,3-丁二烯分子的键线式:
A. 1个 B. 2个 C. 3个 D. 4个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com