
| A.1:1 | B.2:3 | C.3:2 | D.1:6 |
科目:高中化学 来源:不详 题型:单选题
| A.1:1 | B.3:1 | C.3:2 | D.1:3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
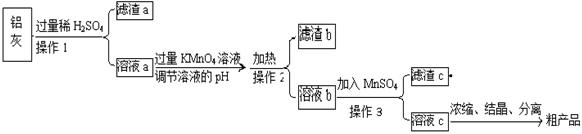
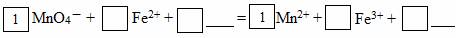
| | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.200mL | B.250ml | C.425mL | D.560mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将水加入浓硫酸中得到稀硫酸,置镁条于其中探究Mg的活泼性 |
| B.将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成 |
| C.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| D.将Mg(OH)2沉淀转入蒸发皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
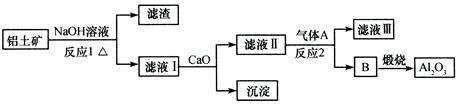
| A.气体A一定为HCl | B.滤液Ⅰ中溶质仅含NaAlO2 |
| C.沉淀的主要成分为硅酸钙 | D.反应1、反应2均不是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 离子 | Mg2+ | Al 3+ | 物质 | Al(OH)3 |
| 开始沉淀pH | 8.93 | 3.56 | 开始溶解pH | 8.04 |
| 完全沉淀pH | 10.92 | 4.89 | 完全溶解pH | 12.04 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
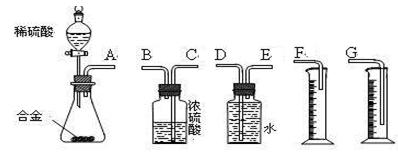
| A.待实验装置冷却后再读数 |
| B.上下移动量筒F,使其中液面与广口瓶中液面相平 |
| C.上下移动量筒G,使其中液面与广口瓶中液面相平 |
| D.视线与凹液面的最低点水平,读取量筒中水的体积 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com