
利用实验器材(规格和数量不限),能完成相应实验的一项是
| 实验器材(省略夹持装置) | 相应实验 |
A | 烧杯、玻璃棒、蒸发皿 | 硫酸铜溶液的浓缩结晶 |
B | 烧杯、玻璃棒、胶头滴管、滤纸 | 用盐酸除去硫酸钡中的少量碳酸钡 |
C | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用固体氯化钠配制0.5mol/L的溶液 |
D | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中的少量NaI |
科目:高中化学 来源:2014-2015学年上海市闵行区八校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列各组微粒中,电子层数和最外层电子数都相同的是
A.F-和Mg2+ B.S和S2- C.Al3+和Ar D.He和H+
查看答案和解析>>
科目:高中化学 来源:2014--2015学年北京市高一上学期期中练习化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是
A.Mg(OH)2和稀硫酸反应:H+ + OH-  H2O
H2O
B.碳酸钡与稀盐酸反应:CO32- + 2H+  CO2↑+ H2O
CO2↑+ H2O
C.澄清石灰水跟盐酸:H+ + OH-  H2O
H2O
D.硫酸溶液与氢氧化钡溶液:H+ +SO42- + Ba2+ + OH-  BaSO4↓+ H2O
BaSO4↓+ H2O
查看答案和解析>>
科目:高中化学 来源:2014--2015学年北京市高一上学期期中练习化学试卷(解析版) 题型:选择题
下列实验操作中不正确的是
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出。
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口处。
C.蒸发时,要用玻璃棒不断搅动溶液
D.过滤时,将待过滤的液体直接倒入漏斗,使液面低于滤纸的边缘。
查看答案和解析>>
科目:高中化学 来源:2013~2014学年福建省第一学期高三第二次月考化学试卷(解析版) 题型:实验题
(15分)某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体 g。
(2)配制过程中需要用到的玻璃仪器除烧杯、玻璃棒外还需要有 、 。
Ⅱ.测定中和热的实验装置如下图所示。
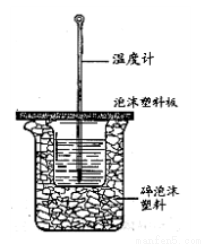
(3)大小烧杯之间填满碎泡沫塑料的作用是 ,从实验装置上看,图中缺少的一种玻璃仪器 。
(4)使用补全仪器后的装置进行实验,取50mL 0.25mol/L H2SO4溶液与50mL0.55 mol/L NaOH溶液在小烧杯中进行中和反应,实验数据如下表。
①请填写下表中的空白:
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ℃ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②通过计算可得中和热△H = (精确到小数点后一位)
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是 。(填字母)
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(5)实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”、“不相等”),所求中和热 (填“相等”、“不相等”);若用50mL0.50mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会 (填“偏大”、“偏小”、“不受影响”)。
查看答案和解析>>
科目:高中化学 来源:2013~2014学年福建省第一学期高三第二次月考化学试卷(解析版) 题型:选择题
常温下,将等质量的铜片、银片、铁片、锌片分别置于四个小烧杯中,然后分别加足量的浓硝酸,放出NO2气体最多的是
A.铜片 B.银片 C.铁片 D.锌片
查看答案和解析>>
科目:高中化学 来源:2013~2014学年福建省第一学期高三第二次月考化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法正确的是
X |
| Y |
|
Z |
| W | Q |
A.钠与Y可能形成Na2Y2化合物
B.由Z与Y组成的物质在熔融时能导电
C.W非金属性比Q强
D.X有多种同素异形体,而Y不存在同素异形体
查看答案和解析>>
科目:高中化学 来源:2013-2014学年浙江省高三上学期期中考试化学试卷(解析版) 题型:选择题
右图所示的装置最适宜于干燥、收集的气体是
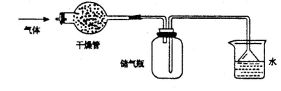
A.NO B.HC1 C.NO2 D.NH3
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省抚顺市六校联合体高一下学期期末考试化学试卷(解析版) 题型:填空题
(共8分)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察右图,然后回答问题。

(1)图中所示反应是_________(填“吸热”或“放热”)反应,该反应________(填“需要” 或“不需要”)加 热,该反应的△H=____________(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+0.5O2(g)=H2O(g) △H=-241.8 kJ/mol;该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为____________________。
(3)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com