
(15分)某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体 g。
(2)配制过程中需要用到的玻璃仪器除烧杯、玻璃棒外还需要有 、 。
Ⅱ.测定中和热的实验装置如下图所示。
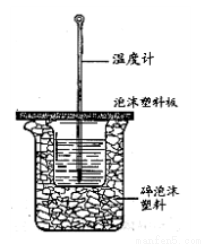
(3)大小烧杯之间填满碎泡沫塑料的作用是 ,从实验装置上看,图中缺少的一种玻璃仪器 。
(4)使用补全仪器后的装置进行实验,取50mL 0.25mol/L H2SO4溶液与50mL0.55 mol/L NaOH溶液在小烧杯中进行中和反应,实验数据如下表。
①请填写下表中的空白:
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ℃ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②通过计算可得中和热△H = (精确到小数点后一位)
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是 。(填字母)
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(5)实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”、“不相等”),所求中和热 (填“相等”、“不相等”);若用50mL0.50mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会 (填“偏大”、“偏小”、“不受影响”)。
Ⅰ.(1)5.0(2分)
(2)250ml容量瓶(1分) 、胶头滴管。(1分)
Ⅱ.(3)保温、隔热、减少实验过程中的热量损失(2分);
环形玻璃搅拌棒或环形玻璃搅拌器。(1分)
(4)①3.4;(1分) ② —56.8kJ/mol(2分) ③A、C、D(2分)
(5)不相等(1分);相等(1分);偏小(1分)。
【解析】
试题分析:Ⅰ.(1)若实验中大约要使用245 mL NaOH溶液,由于与该体积最接近的容量瓶是250mL,因此至少需要称量NaOH固体是(0.50 mol/L×0.25L)×40g/mol=5.0g;(2)配制物质的量浓度的溶液过程中需要用到的玻璃仪器除烧杯、玻璃棒外还需要有250ml容量瓶、胶头滴管;Ⅱ.(3)大小烧杯之间填满碎泡沫塑料的作用是保温、隔热、减少实验过程中的热量损失;从实验装置上看,图中缺少的一种玻璃仪器环形玻璃搅拌棒或环形玻璃搅拌器;(4)①四组实验的温度差值是:3.4℃、6.1℃、3.3℃、3. 5℃,可见第二次实验数据偏差太大,应该舍去,平均温度是:(3.4℃+3.3℃+3. 5℃)÷3=3.4℃,②反应过程中放出的热量Q=c·m·Δt=4.18J/(mol·g·℃)×100g×3.4℃×10-3KJ/J=1.421KJ,n(H+)= 0.05L×0.25mol/L×2=0.025mol;n(OH-)=0.05L×0.55 mol/L=0.02750 mol>0.025mol,所以发生中和反应的物质的量应该以不足量的酸为标准,中和热△H =-Q÷n=-1.421KJ÷0.025mol=—56.8kJ/mol. ③A.实验装置保温、隔热效果差,使热量部分散失,导致中和热偏低,正确;B.量取NaOH溶液的体积时仰视读数,则NaOH的物质的量偏多,使热量产生的多,则中和热偏多,错误; C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中,则在测量过程中热量会部分散失,导致中和热偏低,正确; D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度,则在测量酸时就一部分反应放出,使热量部分散失,导致中和热偏低,正确。因此选项是A、C、D;(5)实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,则n(H+)= 0.06L×0.25mol/L×2=0.003mol>0.02750 mol,所以放出的热量应该以酸为标准;由于反应的物质增多,所以与上述实验相比,所放出的热量就不相等;但是所求中和热由于是产生1mol的水时放出的热量,因此不会发生变化;若用50mL0.50mol/L醋酸代替H2SO4溶液进行上述实验,由于醋酸是弱酸,电离需要吸收热量,因此发生酸碱中和反应放出的热量就少,则测得反应前后温度的变化值会减小。
考点:考查中和热的测定的有关知识,包括数据处理、误差分析、不同物质的影响的知识。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源:2014-2015学年上海市闵行区八校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列物质中,属于纯净物的是
A.盐酸 B.液氯 C.生理盐水 D.漂白粉
查看答案和解析>>
科目:高中化学 来源:2014--2015学年北京市高一上学期期中练习化学试卷(解析版) 题型:选择题
(每空1分,共6分)
写出除去下列物质中的杂质(括号内物质)所用的试剂,并写出发生的离子方程式。
(1)NaOH溶液(Na2CO3) , 。
(2)NaCl溶液(MgCl2) , 。
(3)KCl溶液(CuSO4) , 。
查看答案和解析>>
科目:高中化学 来源:2014--2015学年北京市高一上学期期中练习化学试卷(解析版) 题型:选择题
下列解释实验事实的离子方程式不正确的是
A.Fe与稀H2SO4反应放出气体:Fe + 6H+  2Fe3+ +3H2↑
2Fe3+ +3H2↑
B.稀H2SO4与BaCl2溶液反应生成沉淀:Ba2+ +SO42-  BaSO4↓
BaSO4↓
C.用大理石与稀盐酸制备CO2:CaCO3 + 2H+  Ca2+ + CO2↑+ H2O
Ca2+ + CO2↑+ H2O
D.碳酸钠溶液与足量稀盐酸:CO32- + 2H+  CO2↑+ H2O
CO2↑+ H2O
查看答案和解析>>
科目:高中化学 来源:2014--2015学年北京市高一上学期期中练习化学试卷(解析版) 题型:选择题
用特殊方法把固体物质加工到纳米级(1nm~100nm)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子的大小和这种纳米粒子大小具有相同的数量级的是
A.溶液 B.悬浊液 C.胶体 D.乳浊液
查看答案和解析>>
科目:高中化学 来源:2013~2014学年福建省第一学期高三第二次月考化学试卷(解析版) 题型:选择题
利用实验器材(规格和数量不限),能完成相应实验的一项是
| 实验器材(省略夹持装置) | 相应实验 |
A | 烧杯、玻璃棒、蒸发皿 | 硫酸铜溶液的浓缩结晶 |
B | 烧杯、玻璃棒、胶头滴管、滤纸 | 用盐酸除去硫酸钡中的少量碳酸钡 |
C | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用固体氯化钠配制0.5mol/L的溶液 |
D | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中的少量NaI |
查看答案和解析>>
科目:高中化学 来源:2013~2014学年福建省第一学期高三第二次月考化学试卷(解析版) 题型:选择题
下列说法或表示方法正确的是( )
A.反应物总能量低于生成物总能量时,该反应不能发生
B.稀的强酸与稀的强碱反应放出的热量就是中和热
C.由C(石墨)(s)→C(金刚石)(s);△H>0可行,石墨比金刚石稳定
D.在101kPa,25℃时,2gH2完全燃烧生成液态水,放出285.8kJ的热量;氢气燃烧热的热化学方程式表示为:2H2(g)+ O2(g)= 2H2O(1);△H=-285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源:2013-2014学年浙江省高三上学期期中考试化学试卷(解析版) 题型:选择题
金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应为
aTiO2 + bCl2+eC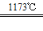 aTiCl4+eCO Ⅰ
aTiCl4+eCO Ⅰ
TiCl4+2Mg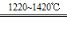 Ti+2MgCl2 Ⅱ
Ti+2MgCl2 Ⅱ
关于反应Ⅰ、Ⅱ的分析不正确的是
①TiCl4在反应Ⅰ中是还原产物,在反应Ⅱ中是氧化剂;②C、Mg在两个反应中均被还原;
③在反应Ⅰ、Ⅱ中Mg的还原性大于C,C的还原性大于TiCl4;
④a=1,b=e =2 ⑤每生成19.2 g Ti,反应Ⅰ、Ⅱ中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②③⑤
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省鞍山市高一下学期期末考试化学(A卷)试卷(解析版) 题型:选择题
下列化学用语正确的是
A.H2O2的电子式: B.丙烷分子的球棍模型:
B.丙烷分子的球棍模型: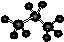
C.CO2的比例模型: D.原子核内有20个中子的氯原子:
D.原子核内有20个中子的氯原子: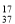 Cl
Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com