
| 事实 | 解释或结论 | |||||
| 1 | 常温下铜、铝均不溶于浓硫酸 | 常温下铜、铝与浓硫酸均不反应 | ||||
| 2 | 测定同浓度的Na2CO3溶液的pH小于Na2SiO2溶液的pH | 水解程度:CO
| ||||
| 3 | 氯水点到蓝色石蕊试纸先变红后褪色 | 氯水中含有H+有酸性、Cl2有漂白性 | ||||
| ④ | 向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| A.①②③④ | B.②③ | C.①②③ | D.①③ |
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源:不详 题型:问答题
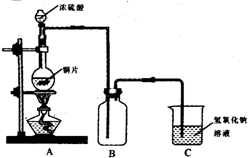
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| Zn的质量 | H2SO4的浓度 | 收集20mLH2所需的时间 | |
| ① | 10g(锌粉) | 0.1mol/L | 125s |
| ② | 10g(锌粉) | 0.2mol/L | 62s |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下浓硫酸与铜反应,浓硫酸体现氧化性和酸性 |
| B.浓硫酸与木炭粉加热发生反应时,浓硫酸只作氧化剂 |
| C.浓硫酸具有吸水性,可用来干燥二氧化硫 |
| D.蔗糖与浓硫酸的作用中,浓硫酸体现脱水性和氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
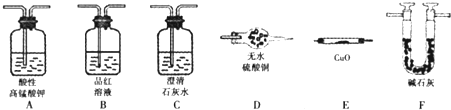
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NO是酸性氧化物 |
| B.NO只能通过人工合成 |
| C.NO是大气污染物,会形成酸雨 |
| D.NO可以用向下排空气法收集 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com