
【题目】下列各组离子在溶液中可以大量共存,加入氢氧化钠溶液后也不产生沉淀的是( )
A.Na+、Ba2+、Cl-、SO42-B.K+、Na+、NO3-、OH-
C.H+ 、NH4+、Fe3+、SO42-D.H+、Cl-、CO32-、NO3-
 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
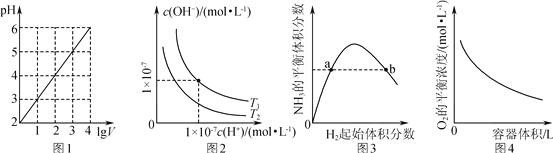
A. 图1表示1 L pH=2的CH3COOH溶液加水稀释至V L,pH随lg V的变化
B. 图2表示不同温度下水溶液中H+和OH-浓度的变化的曲线,图中温度T2>T1
C. 图3表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率小于b点
D. 图4表示同一温度下,在不同容积的容器中进行反应2BaO2(s) ![]() 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
温 度(℃) | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①由上表数据可知该反应为_____ (填放热,吸热,无法确定 )反应。
②下列措施能用勒夏特列原理解释是_____(填序号)。
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500°C左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol氨气溶于水后再与含有0.2mol硫酸的溶液反应放热QkJ,请你用热化学方程式表示其反应式_____。
(3)常温时,将amol氨气溶于水后,再通入bmol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl﹣),则一水合氨的电离平衡常数Kb=_____(用ab表示)。
(4)原料气H2可通过反应 CH4(g)+H2O (g)![]() CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的![]() 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:

①图中,两条曲线表示压强的关系是:P1_____P2(填“>”、“=”或“<”)。
②其它条件一定,升高温度,氢气的产率会__(填“增大”,“减小”减小,“不变”不变)。
(5)原料气H2还可通过反应CO(g)+H2O(g)![]() CO2(g)+H2(g)获取。
CO2(g)+H2(g)获取。
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08molL﹣1,该温度下反应的平衡常数K值为_____。
②保持温度仍为T℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是_____(填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体的还原性,装置如图所示,下列说法不合理的是
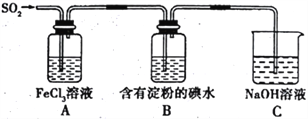
A. 为了验证A 中发生了氧化还原反应,加入稀盐酸酸化的BaCl2溶液,产生白色沉淀
B. 该实验装置至少存在一处设计缺陷
C. 向反应后的A 溶液中加入酸性KMnO4溶液,紫红色褪去,说明一定有Fe2+
D. 装置B是为了验证还原性: SO2>I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电动汽车以锂电池提供动力,锂电池技术已经成为汽车研究的前沿科技某锂电池的电池反应为:xLi+Li3-xNiCoMnO6![]() Li3NiCoMnO6,下列说法正确的是
Li3NiCoMnO6,下列说法正确的是![]()
A. 该电池的充、放电过程互为可逆反应
B. 放电时,电池的负极反应为Li-e-=Li+
C. 放电过程中,Li+向电池的负极移动
D. 该电池可以采用醋酸、乙醇等作为电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列物质的电离方程式:
H2CO3_________________;
NaHCO3_________________;
K2SO4___________________;
NH4NO3__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化铈[Ce(OH)4]是一种重要的稀土化合物。以氟碳铈矿(主要含CeFCO3)为原料制备Ce(OH)4的一种工艺流程如下:
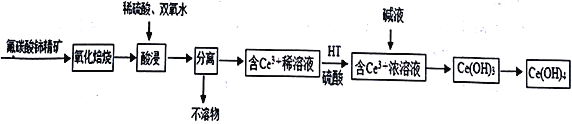
已知:在酸性溶液中Ce4+有强氧化性。回答下列问题:
(1) “氧化焙烧”前需将矿石粉碎成细颗粒,其目的是_________________________,化合物CeFCO3 中Ce 的化合价为________________________。
(2)氧化焙烧生成的铈化合物为二氧化铈(CeO2),其在酸浸时发生反应的离子方程式为__________________________________,酸浸时不宜温度过高的原因是____________________。
(3)已知有机物HT 能将Ce3+从水溶液中萃取出来,该过程可表示为:2 Ce3+ (水层) +6HT (有机层)![]() 2CeT3 (有机层) +6H+ (水层)
2CeT3 (有机层) +6H+ (水层)
从平衡移动角度解释: 向CeT3(有机层) 加入H2SO4获得较纯的含Ce3+的水溶液的原因是____________________。
(4)Ce(OH)3暴露于空气中时变成紫色,最终变成黄色的Ce(OH)4,该反应的化学方程式为________________________________。
(5)已知298 K 时,Ksp[Ce(OH)3]=1×10-20,为了使溶液中Ce3+沉淀完全,需调节pH为______以上。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验:
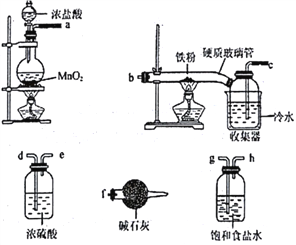
(1)装碱石灰的仪器是____________(填仪器名称),碱石灰的作用______________________。
(2)装置的连接顺序为_________________________。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移
至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
![]()
①固体混合物的成分是_____________________。(填化学式)
②淡黄色溶液中加入试剂X生成淡红色溶液的离子反应方程式为_______________________________。
(4)已知红色褪去的同时有气体生成,经检验为O2。该小组内的同学们对红色褪去的原因提出了三种假设。
假设I:H2O2还原Fe3+,使其转变为Fe2+;
假设Ⅱ:H2O2分解生成O2,O2氧化试剂X;
假设Ⅲ:__________________________________。(如果表达中遇到试剂X,请写出其化学式)。
并对假设进行了以下实验研究:
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
②另取同浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。 实验①说明假设__________不正确; 实验②的目的是_______________;由实验①②得出假设________是正确的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种常用的净水剂,某化学研究小组同学用如图装置制备无水
是一种常用的净水剂,某化学研究小组同学用如图装置制备无水![]() 。已知无水
。已知无水![]() 在空气中易潮解,加热易升华。请回答下列问题:
在空气中易潮解,加热易升华。请回答下列问题:
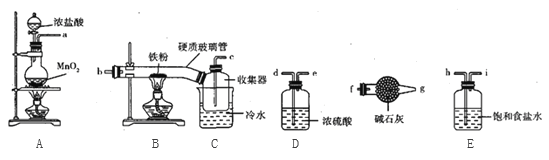
(1)A中发生反应的离子方程式为_________________________________________________。
(2)装置接口的连接顺序为____________________(用a、b、c……i表示);反应开始前应先加热__________处酒精灯(填“A”或“B”)。
(3)装置B中收集器放在冷水中的原因是________________________________________。
(4)反应结束后,该小组同学对B中硬质玻璃管的右端进行加热,其目的是__________。
(5)工业上用5.0mol·![]()
![]() 溶液吸收
溶液吸收![]() 气体,该反应的化学方程式为________________________________________________________;若吸收170g
气体,该反应的化学方程式为________________________________________________________;若吸收170g ![]() 气体,需要该
气体,需要该![]() 溶液的体积为__________L。
溶液的体积为__________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com