
【题目】![]() 是一种常用的净水剂,某化学研究小组同学用如图装置制备无水
是一种常用的净水剂,某化学研究小组同学用如图装置制备无水![]() 。已知无水
。已知无水![]() 在空气中易潮解,加热易升华。请回答下列问题:
在空气中易潮解,加热易升华。请回答下列问题:
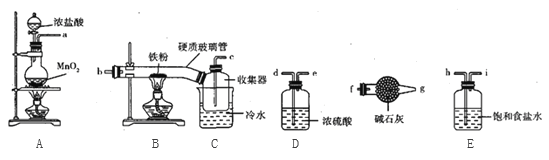
(1)A中发生反应的离子方程式为_________________________________________________。
(2)装置接口的连接顺序为____________________(用a、b、c……i表示);反应开始前应先加热__________处酒精灯(填“A”或“B”)。
(3)装置B中收集器放在冷水中的原因是________________________________________。
(4)反应结束后,该小组同学对B中硬质玻璃管的右端进行加热,其目的是__________。
(5)工业上用5.0mol·![]()
![]() 溶液吸收
溶液吸收![]() 气体,该反应的化学方程式为________________________________________________________;若吸收170g
气体,该反应的化学方程式为________________________________________________________;若吸收170g ![]() 气体,需要该
气体,需要该![]() 溶液的体积为__________L。
溶液的体积为__________L。
【答案】 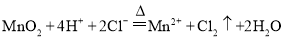 ahidebcf A 冷却使
ahidebcf A 冷却使![]() 沉积,便于收集 使沉积在硬质玻璃管右端的
沉积,便于收集 使沉积在硬质玻璃管右端的![]() 进入收集器
进入收集器 ![]() 2
2
【解析】(1)根据装置图,A中是浓盐酸与二氧化锰反应制备氯气的装置,发生反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)根据装置图,A是氯气的制备装置,B是氯化铁的生成装置,生成的氯气中含有水蒸气和氯化氢杂质,需要用饱和食盐水和浓硫酸除去,最后未反应的氯气需要除去,防止污染空气,氯化铁易潮解,需要防止外界水蒸气进入装置,因此装置接口的连接顺序为ahidebcf;反应开始前应该首先加热A处酒精灯,用生成的氯气将装置中的空气排出,故答案为:ahidebcf;A;
(3) 无水FeCl3在空气中易潮解,加热易升华,因此装置B中收集器需要放在冷水中冷却使FeCl3沉积,便于收集,故答案为:冷却使FeCl3沉积,便于收集;
(4) 无水FeCl3加热易升华,反应结束后,该小组同学对B中硬质玻璃管的右端进行加热,可以使沉积在硬质玻璃管右端的FeCl3进入收集器,故答案为:使沉积在硬质玻璃管右端的FeCl3进入收集器;
(5)工业上用5.0mol/L FeCl3溶液吸收H2S气体,氯化铁将硫化氢氧化生成氯化亚铁和硫,反应的化学方程式为![]() ;若吸收170gH2S气体的物质的量为
;若吸收170gH2S气体的物质的量为![]() =5mol,需要该FeCl3溶液的体积为
=5mol,需要该FeCl3溶液的体积为![]() =2L,故答案为:
=2L,故答案为: ![]() ;2。
;2。


科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中可以大量共存,加入氢氧化钠溶液后也不产生沉淀的是( )
A.Na+、Ba2+、Cl-、SO42-B.K+、Na+、NO3-、OH-
C.H+ 、NH4+、Fe3+、SO42-D.H+、Cl-、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可以获得淡水、食盐并可提取镁和溴等物质.
(1)海水淡化的方法主要有_____________、电渗析法、________________ 。
(2)必须经过化学变化才能从海水中获得的物质是(填序号)_____________.
A.氯、溴、碘 B.钠、镁、铝 C.烧碱、氢气 D.食盐、淡水
(3)从海水中提取镁的流程如图所示:
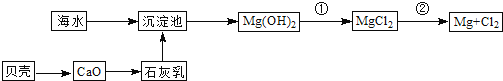
反应②的化学方程式为_________________________________________________。
(4)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化生成溴。向溴单质的水溶液中通入空气和水蒸气将溴单质吹入盛有SO2溶液的吸收塔,其目的是_________,该反应的化学方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分, 请参照元素①~⑧在表中的位置, 用化学用语回答下列问题:

(1)④、⑤、⑥的原子半径由大到小的顺序为______ ___ (填元素符号)。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_____ (填化学式)。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物, 写出其中一种化合物的电子式: ______________________________。
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解, 可使用的催化剂为(填序号)_________________。
a.MnO2b.FeCl3c.Na2SO3d.KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关化学与生产、生活相关的叙述正确的是( )
A.碘酒能消毒是利用碘的还原性
B.葡萄糖注射液不能产生丁达尔效应,不属于胶体
C.14C可用于文物的年代鉴定,14C与12C互为同素异形体
D.某溶液中加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑。下列说法错误的是
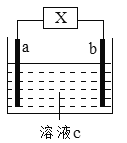
A. a、b不可能是同种材料的电极
B. X为电流计,c为稀盐酸,该装置为原电池
C. X为直流电源,c为稀硫酸,该装置为电解池
D. X为电流计,c为稀硫酸,a可能为铜电极,b可能为锌电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.1 mol H2SO4 的质量为98 gmol﹣1
B.H2SO4的摩尔质量为98 g
C.9.8 g H2SO4含有NA个H2SO4分子
D.6.02×1023个H2SO4分子的质量为98 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠的叙述中,错误的是( )
A.通常情况下钠是固体,密度比水的小比煤油大
B.自然界中无单质钠存在
C.钠在空气中燃烧生成过氧化钠
D.实验后剩余的少量的钠丢入废液缸中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验。下列叙述中不正确的是
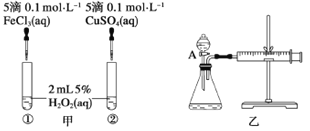
A. 图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小
B. 若图甲实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C. 用图乙所示装置测定反应速率,可测定反应产生的气体体积及反应时间
D. 为检查图乙所示装置的气密性,可关闭A处活塞。将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com