
【题目】为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验。下列叙述中不正确的是
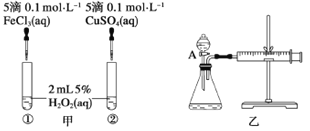
A. 图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小
B. 若图甲实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C. 用图乙所示装置测定反应速率,可测定反应产生的气体体积及反应时间
D. 为检查图乙所示装置的气密性,可关闭A处活塞。将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
【答案】B
【解析】
试题A.反应的剧烈程度与实验现象有关,反应越剧烈,产生气体的速率越快,产生气泡越快,所以正确;B.催化剂能改变化学反应的速率,这里是加快速率,若图1所示实验中反应速率为①>②,则一定说明氯化铁比硫酸铜催化效果好,因二者所含的阴离子不同,要证明Fe3+比Cu2+对H2O2分解催化效果好,还要使选择的试剂中阴离子种类相同,错误.C.反应速率可用单位时间内产生的气体体积表示,该装置可通过注射器活塞的位置变化看生成气体的体积,正确.D.检查装置的气密性一般是利用气压的原理,在图2装置中,关闭A处活塞,将注射器的活塞拉出一定距离,过一段时间后再松开活塞,如活塞回到原位,说明气密性良好,否则漏气,正确。


科目:高中化学 来源: 题型:
【题目】![]() 是一种常用的净水剂,某化学研究小组同学用如图装置制备无水
是一种常用的净水剂,某化学研究小组同学用如图装置制备无水![]() 。已知无水
。已知无水![]() 在空气中易潮解,加热易升华。请回答下列问题:
在空气中易潮解,加热易升华。请回答下列问题:
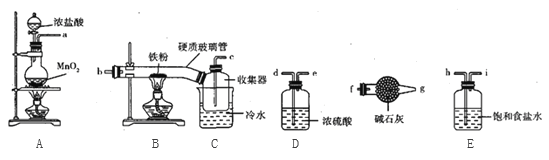
(1)A中发生反应的离子方程式为_________________________________________________。
(2)装置接口的连接顺序为____________________(用a、b、c……i表示);反应开始前应先加热__________处酒精灯(填“A”或“B”)。
(3)装置B中收集器放在冷水中的原因是________________________________________。
(4)反应结束后,该小组同学对B中硬质玻璃管的右端进行加热,其目的是__________。
(5)工业上用5.0mol·![]()
![]() 溶液吸收
溶液吸收![]() 气体,该反应的化学方程式为________________________________________________________;若吸收170g
气体,该反应的化学方程式为________________________________________________________;若吸收170g ![]() 气体,需要该
气体,需要该![]() 溶液的体积为__________L。
溶液的体积为__________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中两个化学反应,属于同一反应类型的一组是
A. 由苯制溴苯;由乙醇与乙酸反应制乙酸乙酯
B. 由乙烯制1,2-二溴乙烷;由乙烷制一氯乙烷
C. 乙烯使溴水褪色;乙烯使酸性高锰酸钾溶液褪色
D. 由苯制硝基苯;由苯制环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种用于合成药物的中间体,其合成路线流程图如下:

(1)B中的含氧官能团名称为羟基、________________和________________。
(2)B→C的反应类型为________________。
(3)写出同时满足下列条件的A的一种同分异构体的结构简式:________________。
①含有苯环,且遇FeCl3溶液不显色;
②能发生水解反应,水解产物之一能发生银镜反应,另一水解产物分子中只有3种不同化学环境的氢。
(4)F 的分子式为C18H20O4,写出F的结构简式:________________。
(5)以苯、甲醛和丙酮为基础有机原料,制备 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。___________________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用锌冶炼废渣(ZnSO4、CuSO4、FeSO4、FeS2、Al2O3、SiO2)制备ZnSO4和Fe2O3的实验流程如下:

已知:“碱浸”时,NaOH溶液浓度越大越粘稠,越容易生成铝硅酸钠沉淀。
(1) “水浸”阶段需在70~80℃条件下进行,适宜的加热方式为________________。
(2)“氧化”阶段是将Fe2+氧化后进一步生成Fe(OH)3,从反应产物的角度分析,以氯水替代H2O2的缺点是①使ZnSO4中混有ZnCl2;②________________。
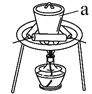
(3)“灼烧”时FeS2发生反应的化学方程式为________________。使用的装置如右图,仪器a的名称为________________。
(4) “碱浸”阶段,在其它条件不变的情况下,所得固体中Fe2O3含量随NaOH溶液的浓度的增大而增大,但当氢氧化钠浓度大于12 mol·L-1时,Fe2O3含量反而降低,其原因是________________。
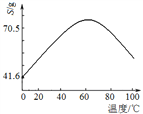
(5)“滤液Ⅰ”溶质主要是ZnSO4和CuSO4。已知硫酸锌晶体的溶解度随温度变化如右图,请设计从“滤液Ⅰ”中获取ZnSO4晶体的实验方案:________________(实验中须使用的试剂有:Zn粉、稀H2SO4、酒精)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废水废气对自然环境有严重的破坏作用,大气和水污染治理刻不容缓。
(1)某化工厂产生的废水中含有Fe2+、Mn2+等金属离子,可用过硫酸铵[(NH4)2S2O8]氧化除去。
①过硫酸铵与Mn2+反应生成MnO2的离子方程式为________________。
②温度与Fe2+、Mn2+氧化程度之间的关系如图1所示:

图1
实验过程中应将温度控制在________________。Fe2+与Mn2+被氧化后形成胶体絮状粒子,常加入活性炭处理,加入活性炭的目的为________________。
③H2O2也有较强氧化性,在实际生产中不用H2O2氧化Mn2+的原因是________________。
(2)利用某分子筛作催化剂,NH3可脱除废气中NO、NO2,其反应机理如图2所示。A包含物质的化学式为N2和________________。


图2 图3
(3)工业上废气中SO2可用Na2CO3溶液吸收,反应过程中溶液组成变化如图3所示。
①吸收初期(图中A点以前)反应的化学方程式为________________。
②C点高于B点的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3与KI溶液反应生成的两种单质是______________和________________(填分子式)。
(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如下表所示。已知:O3的起始浓度为0.0216 mol/L。
T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
20 | 301 | 231 | 169 | 58 |
30 | 158 | 108 | 48 | 15 |
50 | 31 | 26 | 15 | 7 |
①pH增大能加速O3分解,表明对O3分解起催化作用的是________。
②在30 ℃、pH=4.0条件下,O3的分解速率为________mol/(L·min)。
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为________(填字母代号)。
a.40 ℃、pH=3.0
b.10 ℃、pH=4.0
c.30 ℃、pH=7.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质。请回答:
(1)甲烷的电子式为 ______________,空间构型为_____________。
(2)下列可以鉴别甲烷和乙烯的试剂为________(填选项字母)。
A.稀硫酸 B.溴的四氯化碳溶液
C.水 D.酸性高锰酸钾溶液
(3)写出下列化学方程式,并指出反应类型:
CH4与Cl2光照生成CH3Cl_____________________________,反应类型________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施对增大反应速率明显有效的是( )
A.Na与无水乙醇反应时增大无水乙醇的用量
B.Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸
C.在K2SO4与BaCl2两溶液反应时,增大压强
D.将炭块磨成炭粉用于燃烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com