
����Ŀ����ˮ��������Ȼ���������ص��ƻ����ã�������ˮ��Ⱦ�����̲��ݻ���
��1��ij�����������ķ�ˮ�к���Fe2����Mn2+�Ƚ������ӣ����ù������[(NH4)2S2O8]������ȥ��
�ٹ��������Mn2+��Ӧ����MnO2�����ӷ���ʽΪ________________��
���¶���Fe2+��Mn2+�����̶�֮��Ĺ�ϵ��ͼ1��ʾ��

ͼ1
ʵ�������Ӧ���¶ȿ�����________________��Fe2+��Mn2+���������γɽ�����״���ӣ����������̿�������������̿��Ŀ��Ϊ________________��
��H2O2Ҳ�н�ǿ�����ԣ���ʵ�������в���H2O2����Mn2+��ԭ����________________��
��2������ij����ɸ��������NH3���ѳ�������NO��NO2���䷴Ӧ������ͼ2��ʾ��A�������ʵĻ�ѧʽΪN2��________________��


ͼ2 ͼ3
��3����ҵ�Ϸ�����SO2����Na2CO3��Һ���գ���Ӧ��������Һ��ɱ仯��ͼ3��ʾ��
�����ճ��ڣ�ͼ��A����ǰ����Ӧ�Ļ�ѧ����ʽΪ________________��
��C�����B���ԭ����________________��
���𰸡� S2O82�� + 2H2O + Mn 2��=4H�� + 2SO42�� + MnO2�� 80����80��~90����������� �������������γɳ��� �̵Ļ�����ɴ�H2O2�ķֽ���ʹ���ĵ�H2O2���� H2O 2Na2CO3 + SO2 + H2O��2NaHCO3 + Na2SO3 ������Ԫ���غ��� NaHSO3�����ʵ�����Na2CO3��2��������NaHSO3�������������������ʹ�
����������1���ٹ��������Mn2+��Ӧ����MnO2������������ԭΪSO42������Ӧ�����ӷ���ʽΪS2O82�� + 2H2O + Mn 2��=4H�� + 2SO42�� + MnO2�����ڸ���ͼ1��֪��80��ʱFe2+��Mn2+�����̶Ƚӽ�1.0����ʵ�������Ӧ���¶ȿ�����80����Fe2+��Mn2+���������γɽ�����״���ӣ����������̿�������������̿��Ŀ��Ϊ�������������γɳ�������H2O2Ҳ�н�ǿ�����ԣ���ʵ�������в���H2O2����Mn2+��ԭ�����̵Ļ�����ɴ�H2O2�ķֽ���ʹ���ĵ�H2O2���ࣻ��2������ͼʾ��Ӧ�ɲ���A�ķ�ӦΪ��[��NH4����HNO2��]+=N2+A+H+����Ϸ�Ӧ���Ƶ���AΪH2O����ӦΪ[��NH4����HNO2��]+=N2+ 2H2O +H+����3�������ճ��ڣ�ͼ��A����ǰ����ҵ�Ϸ�����SO2����Na2CO3��Һ���գ���ͼ����Ϣ��֪��NaHCO3 ��Na2SO3�����������ӣ�������Ӧ�Ļ�ѧ����ʽΪ��2Na2CO3 + SO2 + H2O��2NaHCO3 + Na2SO3����C�����B���ԭ���Ǹ�����Ԫ���غ��� NaHSO3�����ʵ�����Na2CO3��2��������NaHSO3�������������������ʹ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ���з�����Ӧ�����ӷ���ʽΪ��Zn+2H+��Zn2++H2��������˵���������
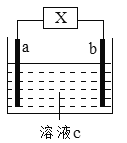
A. a��b��������ͬ�ֲ��ϵĵ缫
B. XΪ�����ƣ�cΪϡ���ᣬ��װ��Ϊԭ���
C. XΪֱ����Դ��cΪϡ���ᣬ��װ��Ϊ����
D. XΪ�����ƣ�cΪϡ���ᣬa����Ϊͭ�缫��b����Ϊп�缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ͻ���������Ļ�е���ܣ���;�㷺���������ʲ����ںϽ����
A. ���� B. ʯӢ C. ����� D. ��ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Һ�У�Cl-���ʵ���Ũ�������ǣ� ��
A.5L 0.4mol��L-1 NaCl��ҺB.4L 0.5mol��L-1 MgCl2��Һ
C.1L 0.3mol��L-1 AlCl3��ҺD.10L 0.5mol��L-1 NaCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�Ƚ�Fe3+��Cu2+��H2O2�ֽⷴӦ�Ĵ�Ч�����ס�����λͬѧ�ֱ��������ͼ�ס�����ʾ��ʵ�顣���������в���ȷ����
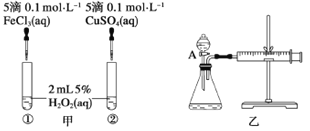
A. ͼ����ʾʵ���ͨ���۲�������ݵĿ������ȽϷ�Ӧ���ʵĴ�С
B. ��ͼ��ʵ���з�Ӧ����Ϊ�٣��ڣ���һ��˵��Fe3+��Cu2+��H2O2�ֽ��Ч����
C. ��ͼ����ʾװ�òⶨ��Ӧ���ʣ��ɲⶨ��Ӧ�����������������Ӧʱ��
D. Ϊ���ͼ����ʾװ�õ������ԣ��ɹر�A����������ע������������һ�����룬һ��ʱ����ɿ��������۲�����Ƿ�ص�ԭλ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ͼ��

���з�Ӧ��ͬʱ������������ͼ�����
A. 2HI(g)![]() H2(g)+I2(g) ��H>0
H2(g)+I2(g) ��H>0
B. 2SO2(g)+O2(g)![]() 2SO3(g) ��H<0
2SO3(g) ��H<0
C. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ��H<0
4NO(g)+6H2O(g) ��H<0
D. N2O4(g)![]() 2NO2(g) ��H>0
2NO2(g) ��H>0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����Һ�����廯���Ĵ������¿��Է�����Ӧ�����屽��ij��ѧ����С������ͼ��ʾװ����ȡ�屽��֤�������巢������ȡ����Ӧ�������Һ©���м��뱽��Һ�壬�ٽ����Һ�������뷴Ӧ��A��A�¶˻����رգ��С���֪��������屽�С�

��1��д��A�з�Ӧ�Ļ�ѧ����ʽ��__________��
��2��ʵ��ʱ�ɹ۲쵽A�з������ҷ�Ӧ����ӦҺ�������к���ɫ�������������A������˵��������ķ�Ӧ��__________��Ӧ������ȡ������ȡ�����
��3��ʵ�����ʱ����A�¶˵Ļ������÷�ӦҺ����B�У������Ŀ����__________��д���йصĻ�ѧ����ʽ__________��
��4��C��ʢ��CCl4��������__________��
��5�����Թ�D�м���AgNO3��Һ������������ɫ����������֤�������巢������ȡ����Ӧ�����Ǽӳɷ�Ӧ����һ��֤�����������Թ�D�м���__________��������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥCO2�л��е�����SO2���壬���ѡ�õ��Լ��ǣ� ��
A.����ʯ��ˮ
B.Ʒ����Һ
C.NaOH��Һ
D.����NaHCO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�·����ϳɷ֣���72%��������ά28%������˵����ȷ����
A. ������Ҫ�ɷ�Ϊ��ά��
B. ������ά������Ȼ��ά
C. ϴ�Ӹ��·����ʺ��ü�øϴ�Ӽ�
D. ���·������ֳɷ־����ںϳɲ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com