
图为相互串联的甲、乙两电解池.试回答:

(1)若甲电解池利用电解原理在铁上镀银,则A是 (填电极材料),电极反应式 ;B(要求同A)是 ,电极反应式 ;应选用的电解质溶液是 。
(2)乙电解池中若滴入少量酚酞试液,开始电解一段时间,铁极附近呈 ,C极附近呈 。
(3)若甲电解池阴极增重4.32g,则乙槽中阳极上放出的气体在标准状况下的体积是 。
(4)若乙电解池中剩余溶液仍为400mL,则电解后所得溶液中新生成溶质的物质的量浓度为 mol?L-1,溶液的pH等于 。
(1)铁、阴极,Ag++e-═Ag;银、阳极、Ag-e-═Ag+; 硝酸银溶液。
(2)红;浅黄绿
(3)448mL
(4)0.1mol/L;13
【解析】(1)甲池是电镀池,铁作阴极,银作阳极,阴极上银离子得电子发生还原反应,电极反应式为Ag++e-═Ag,阳极上银失电子发生氧化反应,电极反应式为Ag-e-═Ag+,电解质溶液为可溶性的硝酸银溶液。
(2)乙是电解池,碳电极上氯离子放电生成氯气,铁电极上氢离子放电生成氢气,同时溶液中生成氢氧根离子,导致铁电极附近溶液呈碱性,酚酞试剂遇碱变红色,所以铁电极附近溶液变红色,碳电极上生成氯气,氯气是浅黄绿色气体,溶于水而使溶液呈浅黄绿色,所以C电极附近呈浅黄绿色。
(3)甲池中阴极上析出银,若甲电解池阴极增重4.32g,转移电子的物质的量=4.32g÷108g/mol=0.04mol,乙池中阳极上生成氯气,生成1mol氯气转移电子的物质的量是2mol,当转移0.04mol电子时生成氯气的物质的量为0.02mol,则氧气体积=0.02mol×22.4L/mol=0.224L=448mL。
(4)乙池中电池反应式为2NaCl+2H2O H2↑+Cl2↑+2NaOH,根据氯气和氢氧化钠的关系式知,生成0.02mol氯气时同时生成0.04mol氢氧化钠,则氢氧化钠的物质的量浓度=0.04mol÷0.4L=0.1mol/L,则溶液中氢离子浓度=10?14/0.1
H2↑+Cl2↑+2NaOH,根据氯气和氢氧化钠的关系式知,生成0.02mol氯气时同时生成0.04mol氢氧化钠,则氢氧化钠的物质的量浓度=0.04mol÷0.4L=0.1mol/L,则溶液中氢离子浓度=10?14/0.1
mol/L=10-13 mol/L,所以其pH=13。


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源:2014高考名师推荐化学--预测15 题型:实验题
工业上以黄铜矿(主要成分是CuFeS2,杂质不溶于水和酸)为原料,制备蓝色晶体G,其化学式为[Cu(NH3)4]SO4·H2O,涉及流程如下:
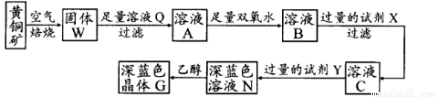
已知25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表:
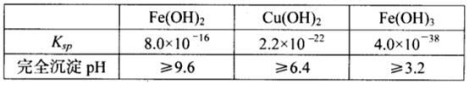
(1)黄铜矿在空气中焙烧能生成铁和铜的低价硫化物,写出其反应的化学方程式 ;
(2)试剂X的化学式为 ,双氧水的作用是 ;
(3)常温下,0.1 mol/L试剂Y的pH=11,则该温度下,试剂Y的电离常数为 ,用pH试纸测该溶液pH值的方法是 ;
(4)在溶液N中加入乙醇的目的是 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测14 题型:选择题
下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是
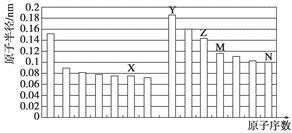
A.Z、N两种元素的离子半径相比,前者较大
B.X、N两种元素的气态氢化物的沸点相比,前者较低
C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测13 题型:选择题
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验:

A.步骤Ⅰ中减少的3 g固体一定是混合物
B.步骤Ⅱ中质量减少的物质一定是Cu
C.根据步骤Ⅰ、Ⅱ可以判断混合物X的成分为Al2O3、Fe2O3、Cu、SiO2
D.根据上述步骤Ⅱ可以得出m(Fe2O3)∶m(Cu)=1∶1
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测12 题型:选择题
X、Y、Z、W、R是原子序数依次增大的五种短周期元素,化合物XZ、Y2W能破坏水的电离平衡,XR能抑制水的电离,则Y元素为
A.Li B.F C.Na D.S
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测12 题型:选择题
下列说法不正确的是
A.已知H2(g)+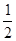 O2(g)===H2O(g) ΔH1=a kJ·mol-1;
O2(g)===H2O(g) ΔH1=a kJ·mol-1;
2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1,则a>b
B.CO的燃烧热为283.0 kJ·mol-1,则
2CO2(g)===2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1
C.若N2(g)+3H2(g)  2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
D.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和KOH反应的中和热ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测11 题型:选择题
下列有关说法正确的是
A、氨水稀释后,溶液中 的值减小
的值减小
B、 0.1 mol·L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小
C、电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等
D、 298 K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其ΔH>0
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测1 题型:选择题
25℃时,水的离子积常数为Kw,该温度下a mol?L-1的HA与bmol?L-1强碱BOH等体积混合,若恰好完全中和,下列结论中不正确的是
A.混合液中:c(H+)≤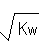
B.混合液中:c(HA)+c(A-)=amol?L-1
C.a=b
D.混合液中:c(H+)+c(B+)=c(OH-)+c(A-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com