
 CH3CH2OH(g)+H2O(g)�����ܱ������г���10 mol CO��20mol H2���ڴ��������·�Ӧ�����Ҵ���CO��ת����(��)���¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
CH3CH2OH(g)+H2O(g)�����ܱ������г���10 mol CO��20mol H2���ڴ��������·�Ӧ�����Ҵ���CO��ת����(��)���¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��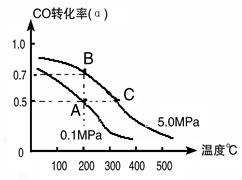
 CH3OH(g)��H2O(g)������6mol CO2��8 mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯����������ͼ��ʾ��ʵ�ߣ���
CH3OH(g)��H2O(g)������6mol CO2��8 mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯����������ͼ��ʾ��ʵ�ߣ���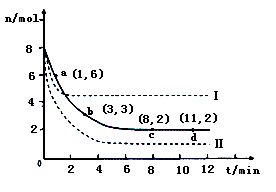

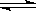 CH3CH2OH(g)+H2O(g)
CH3CH2OH(g)+H2O(g)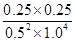 ��0.25��
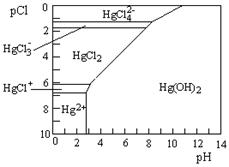
��0.25�� HgCl�� + HgCl3����C����ȷ��D������ͼ���֪����ҺpH������4��pCl��2�ı���6ʱ����ʹHgCl2ת��ΪHg(OH)2��D��ȷ����ѡAD��
HgCl�� + HgCl3����C����ȷ��D������ͼ���֪����ҺpH������4��pCl��2�ı���6ʱ����ʹHgCl2ת��ΪHg(OH)2��D��ȷ����ѡAD��

 ��ѧ��������������Ͼ���ѧ������ϵ�д�
��ѧ��������������Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO(g)��H2O(g)��ƽ�ⳣ�����¶ȱ仯���±���
CO(g)��H2O(g)��ƽ�ⳣ�����¶ȱ仯���±���| t/�� | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
| | A | B | C | D | E |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
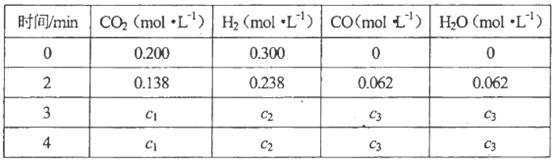
| ʱ�� /min | CO2 (mol��L��1) | H2 (mol��L��1) | CO (mol��L��1) | H2O (mol��L��1) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)�ﵽƽ��״̬��־����(����)��
2C(g)�ﵽƽ��״̬��־����(����)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 (H2O)x(g)����Ӧ�������������ʵ�����ʱ��仯��ϵ��ͼ������˵������ȷ����
(H2O)x(g)����Ӧ�������������ʵ�����ʱ��仯��ϵ��ͼ������˵������ȷ����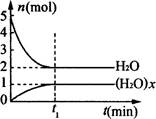
| A��x=3 |
| B�����¶��£���Ӧ��ƽ�ⳣ��Ϊ0.125L3/mol3 |
| C��ƽ��ʱ��������ƽ��Ħ��������33.3g/mol |
| D��t1ʱ�̣������¶Ȳ��䣬�ٳ���1mol H2O(g)�����´ﵽƽ��ʱ��c[(H2O)x]/c[H2O]���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ��ƽ�ⳣ��K���¶ȣ��Ĺ�ϵ���£�
��ƽ�ⳣ��K���¶ȣ��Ĺ�ϵ���£�
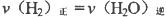 B�����������COŨ�Ȳ���
B�����������COŨ�Ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 N2O4,���в���˵����Ӧ�ﵽ��ƽ��״̬���� (����)
N2O4,���в���˵����Ӧ�ﵽ��ƽ��״̬���� (����)| A��N2O4����������N2O4�ֽ��������ʱ |
| B���������ƽ����Է����������ֲ���ʱ |
| C��NO2�ķ�������N2O4��������Ϊ2��1ʱ |
| D����ϵ��ɫ���ٷ����ı�ʱ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g)����H����a kJ��mol��1(a>0)�����º����£���10 L���ܱ������м���0.1 mol SO2��0.05 mol O2������2 min�ﵽƽ��״̬����Ӧ����0.025 a kJ�������ж���ȷ����(����)
2SO3(g)����H����a kJ��mol��1(a>0)�����º����£���10 L���ܱ������м���0.1 mol SO2��0.05 mol O2������2 min�ﵽƽ��״̬����Ӧ����0.025 a kJ�������ж���ȷ����(����)| A����2 min�ڣ�v(SO2)��0.25 mol��L��1��min��1 |
| B�����ٳ���0.1 mol SO3���ﵽƽ���SO3�������������С |
| C����1 minʱ��c(SO2)��c(SO3)��0.01 mol��L��1 |
| D�������º�ѹ�£���10 L���ܱ������м���0.1 mol SO2��0.05 mol O2��ƽ���Ӧ����С��0.025a kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
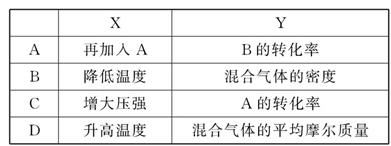
 2C(g) ��H<0���ﵽƽ��ı�һ��������������(Y)�ı仯������ͼ�����ߵ���( )
2C(g) ��H<0���ﵽƽ��ı�һ��������������(Y)�ı仯������ͼ�����ߵ���( )
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com