
| A、称量时,将NaOH固体直接放在天平托盘上面的纸上 |
| B、将称好的NaOH固体直接放入容量瓶中,加入少量水溶解 |
| C、在烧杯中溶解NaOH固体后,立即将所得溶液注入容量瓶中 |
| D、将烧杯中已冷却的NaOH溶液注入容量瓶中 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
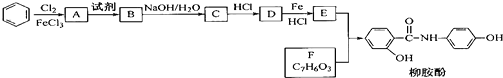
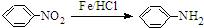 .请回答下列问题:
.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
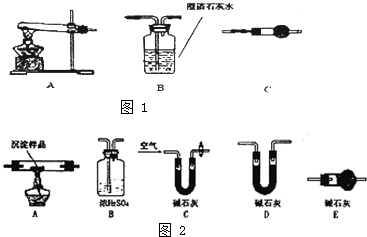 某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.
某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
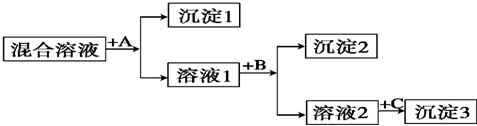
| Ba2+ | Cu2+ | Ag+ | |
| Cl- | 溶 | 溶 | 不 |
| CO | 不 | 不 | 不 |
| SO | 不 | 溶 | 微 |
| S2- | 溶 | 不 | 不 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A、4个 | B、3个 | C、2个 | D、1个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com